基于CRISPR/ cas9的基因组编辑技术彻底改变了实验分子生物学,并进入了靶向基因治疗的临床领域。识别发生在 CRISPR/Cas9 靶位点的 DNA 修饰对于确定编辑工具的效率和安全性至关重要。典型的 CRISPR/Cas9 DNA 编辑会诱导双链断裂 (DSB),双链断裂可通过经典的非同源末端连接修复 (c-NHEJ),并且通常会在靶标位点产生相对较小的 DNA 序列的插入或缺失。在极少数情况下,由 CRISPR/Cas9 诱导的 DSB 会导致更大的基因组重排,例如大的染色体缺失、倒位或易位等。典型CRISPR/Cas9编辑的其他结果包括外源性序列的整合,包括慢病毒、腺相关病毒(AAV)、质粒和小DNA片段。这些事件利用了CRISPR/Cas9产生的频繁DSB,从而有利于通过微同源介导末端连接(MMEJ)插入外源性DNA片段。
虽然已知可以在DSB位点捕获可移动的遗传元件,但对逆转录转座子整合到CRISPR/Cas9编辑位点的频率和机制知之甚少。近日,Nature Communications杂志在线发表了美国波士顿儿童医院暨哈佛医学院病理科Roberto Chiarle团队题为“Frequency and mechanisms of LINE-1 retrotransposon insertions at CRISPR/Cas9 sites”的研究论文。在这项研究中,他们通过PolyA-seq和改进的扩增子测序技术,描述了在三个人类细胞系中,从头 L1RP和L1- orfeus插入到多个典型CRISPR/Cas9编辑位点的发生情况,并使用超过2500个从头L1插入事件的结构来推断潜在的机制。
逆转录转座子是通过逆转录RNA中间体产生从头插入的自我繁殖的序列,LINE-1(L1) 是人类基因组中唯一具有自主转座能力的转座子。在细胞模型中,常用两种不同类型的报告因子来研究L1逆转录转位事件。一个本地L1报告基因(L1RP)使用本地L1RP序列和本地L1 5 UTR启动子来紧密模拟内源性L1逆转录转位,而一个合成的L1报告基因(L1- orfeus)包含一个密码子优化的人类L1序列,该序列可以区分重新生成的L1插入和非活性内源性L1片段的插入。在这里,他们证明了LINE-1 (L1) 反转录转座子的插入可以在 CRISPR/Cas9 编辑位点频繁发生。通过PolyA-seq和一个改进的扩增子测序,他们在HEK293T、HeLa和U2OS细胞中的多个CRISPR/Cas9编辑位点检测到了超过2500个L1从头插入。这些L1逆转录转位事件利用CRISPR/ cas9诱导DSB形成,并需要L1 RT活性。此外,他们发现,在基于crispr的基因组编辑工具(PE和BE)中,不需要形成DSB中间体的从头 L1-ORFeus插入非常罕见,这与它们减少DSB的形成是一致的。这些数据表明,插入逆转录转座子可能是CRISPR/Cas9基因组编辑的一个潜在结果,并为不同的基于CRISPR的编辑工具的安全性提供了进一步的证据。
总体而言,他们的结果表明,L1 元件的逆转录转座是典型 CRISPR/Cas9 编辑的常见结果。尽管这些发现需要在更多生理或临床环境中得到进一步证实,但考虑到 L1 插入的潜在致病作用,当基因编辑用于临床治疗时,应仔细评估它们。
CRISPR/ cas9介导的DSB任一DNA端L1-ORFeus插入的示意图模型
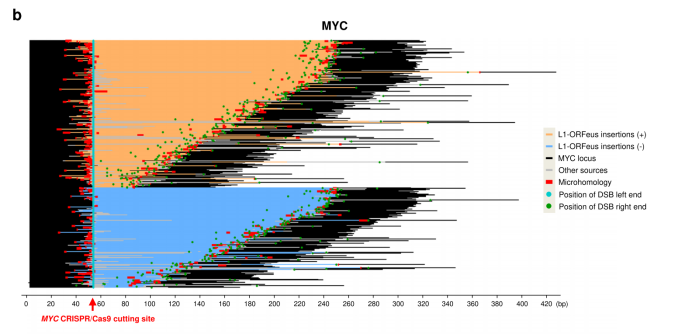
通过扩增子测序获得目标MYC位点的L1- ORFeus连接分析