本文内容速览:
自然界中的植物往往会进化出最有利于生存的有性形态。但从经济学层面上来讲,我们可以通过不同的育种技术,人为选择培育经济价值最高的作物有性形态。例如,对于瓜果类作物雌株或雌花比例高可以提高产量;对于以收获茎叶为目的的作物如雄性芦笋的口感更佳可以优先种植;杨树柳树的雌性在成熟时会产生大量的柳絮,造成环境污染问题,因此可优先种植雄性。接下来小远将给大家介绍植物中几种较为典型的性相关基因,希望可以给大家的科研提供一定的帮助。
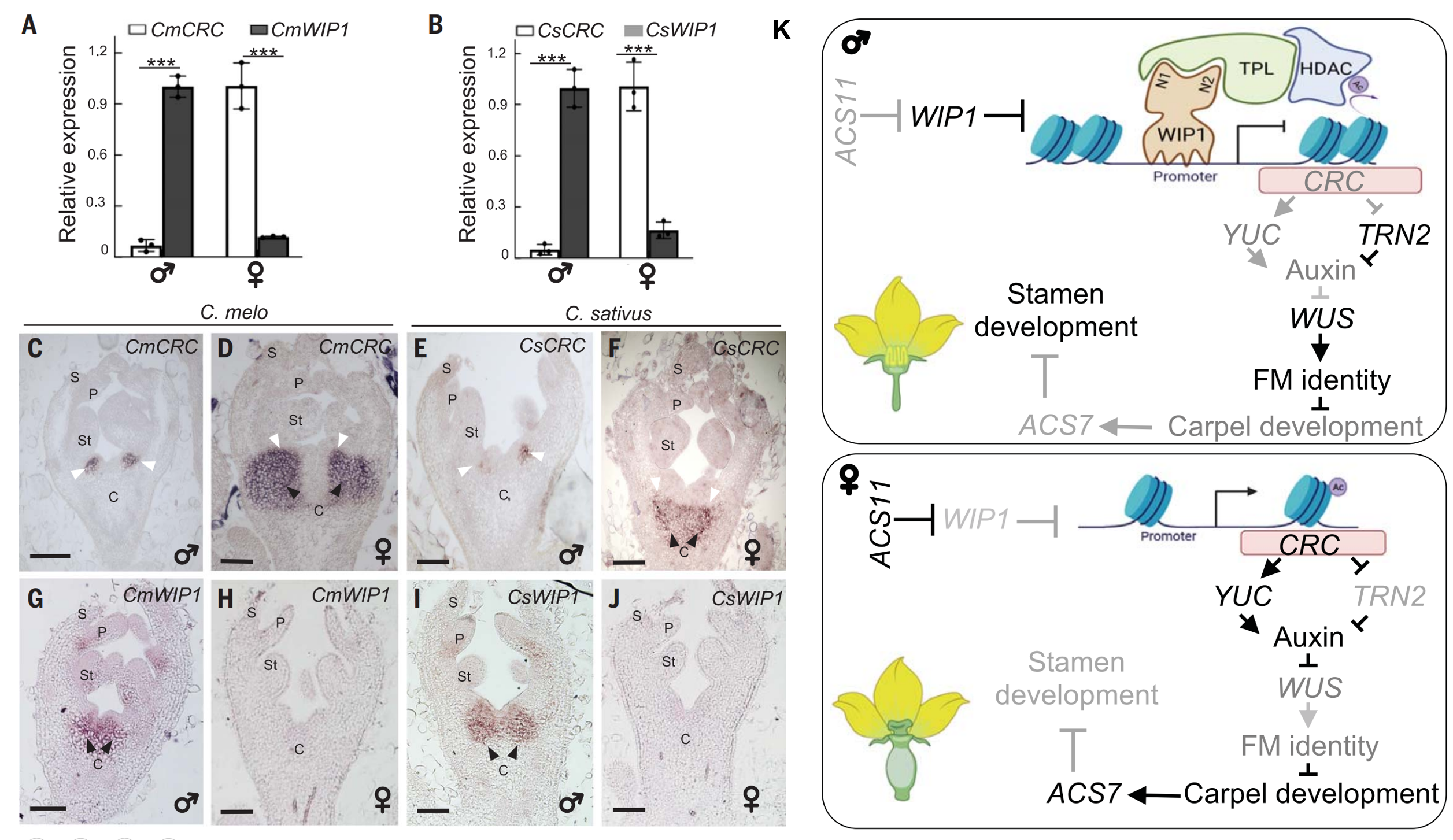
2022年11月,巴黎萨克雷大学Abdelhafid Bendahmane课题组在Science杂志上发表了一篇题为“The control of carpel determinacy pathway leads to sex determination in cucurbits”的研究论文。作者通过正向遗传学筛选发现了甜瓜中由雌花转变为雄花的突变体并将其命名为Little Boy(Lib),对应的基因为YABBY转录因子家族心皮识别基因CRABS CLAW(CRC )(图1A-C)。病毒诱导的基因沉默(VIGS)实验证明,CRC 的沉默可以使雌花转变为雄花,结合筛选甜瓜和黄瓜的TILLING(基因组学中的靶向诱导局部病变 )基因组,发现CRC 纯合功能缺失突变体均表现出雌花到雄花的转变(图1D-H)。
随后作者分析了甜瓜和黄瓜中CRC 的表达量发现CRC 在雌花花蕾中高表达而在雄花花蕾中低表达,原位杂交技术检测CRC 和WIP1(葫芦科性别决定的关键调控因子,其高表达抑制心皮原基发育形成雄花)的空间表达模式发现,二者在心皮原基中表现出拮抗模式。通过一系列的蛋白-蛋白互作及组蛋白乙酰化检测实验证明WIP1通过招募共抑制因子TOPLESS(TPL)结合到CRC 的启动子上,通过组蛋白去乙酰化抑制CRC 的表达,从而使雌花变为雄花(图2)。
图2 CRC介导雄花发育调控网络图(Zhang et al., 2022)。(A、B)CRC 和WIP1的qRT-PCR分析;(C-F)CRC 的原位表达。黑色箭头表示在雌花心皮原基中检测到的CRC 转录本;(G-J)WIP1的原位表达。黑色箭头表示在雄花心皮原基中检测到的CmWIP1和CsWIP1转录本。雌花中未检测到转录本;(K)在单性花中,雄性和雌性促进基因分别为WIP1、ACS7,均可在心皮原基中表达。WIP1通过招募TPL以抑制CRC 的表达,进而干扰心皮的决定性从而诱导雄花发育;而CRC 的表达可促进心皮的决定性,ACS7在心皮决定性后表达并诱导雌花发育。


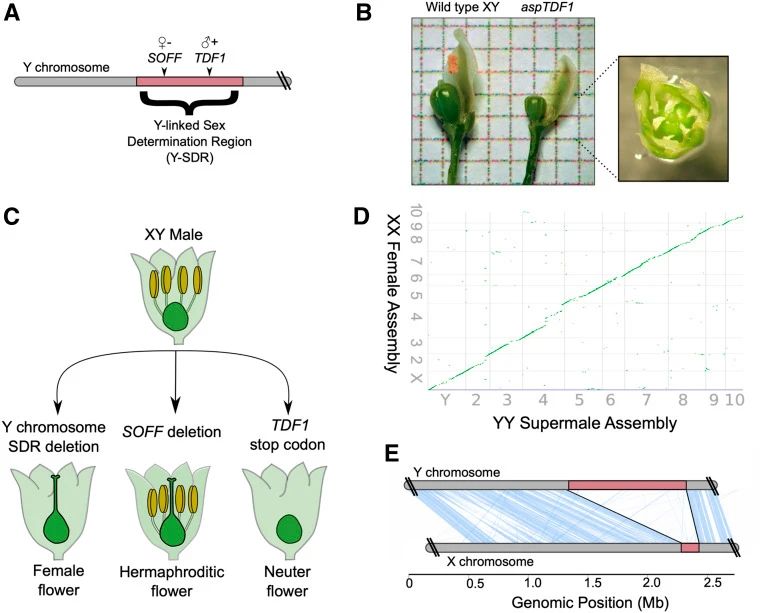
2017年11月,江西省农业科学院蔬菜研究所陈光宇课题组在Nature communications杂志上发表了一篇题为“The asparagus genome sheds light on the origin and evolution of a young Y chromosome”的研究论文,作者对超雄芦笋(染色体组成为YY)进行全基因组测序,发现在Y染色体上存在一个1M左右的非重组雄性特异性的性别决定区域(Y-SDR)。分析该区域发现,存在一个DEFECT IN TAPETUM DEVELOPMENT AND FUNCTION 1(TDF1)基因,在拟南芥中敲除TDF1会导致雄性不育,异源回补AspTDF1则可以弥补这一变化。随后对EMS诱变产生的可结实的突变体植株进行分析发现,其花均是雌雄同体的,基因组重测序表明局部突变仅限于包含DUF247 结构域的单个Y 特异性基因,RNA-seq分析和包含Y 连接的DUF247 结构域的基因的靶向测序确定了该基因并将其命名为SUPPRESSOR OF FEMALE FUNCTION(SOFF )。
随后2020年佐治亚大学Jim Leebens-Mackb课题组在此研究基础上通过EMS诱变敲除整个Y-SDR,导致芦笋从雄性转变为雌性,敲除SOFF会导致染色体组成为XY的雄性芦笋转变为雌雄同体(Harkess et al., 2020)。表明芦笋中的Y染色体通过两个Y连锁基因(SOFF 和TDF1)决定性别,其中SOFF抑制雌性雌蕊的发育,TDF1促进雄性花药的发育(图8)。
图8 芦笋Y染色体的结构和性别决定功能及其相对于X染色体的结构变异(Harkess et al., 2020)。(A)Y染色体端粒区和近1MbSDR的描述;(B)XY野生型和EMS诱变敲除TDF1的植株表型;(C)编辑Y-SDR可以实现芦笋的性别转换。
图9 SyGI 的功能验证(Akagi ey al., 2018)。(A-D)过表达SyGI 拟南芥花的表型特征。与对照植物(A、C)相比,转基因植株(B、D)表现出具有短花柱(St)和萎缩柱头(Sg)的未成熟心皮(RC)。An:花药,Se:萼片;(E)野生型拟南芥和pSyGI-SyGI 转基因植株之间的相互杂交,pSyGI-SyGI 转基因植物可以作为父本,作为母本则不育。Si:长角果,NL:不育豆科植物;(F-I)过表达SyGI 烟草花的表型特征;(J-L)野生型烟草和pSyGI-SyGI 转基因烟草成熟花柱头的比较;(M-O)野生型烟草(M)和pSyGI-SyGI 转基因烟草(N、O)授粉后的花粉管苯胺蓝染色;(Q-S)野生型烟草(Q)和pSyGI-SyGI 转基因烟草(R)的花粉形态和发芽率统计(S)。
紧随其后,该团队2019年8月在Nature plants杂志上发表了一篇题为“Two Y-chromosome-encoded genes determine sex in kiwifruit”的研究论文,作者揭示了猕猴桃的第二个性别决定基因Friendly Boy(FrBy),作者分别在拟南芥和烟草中编辑了FrBy的同源基因,均发现编辑突变体的花粉发芽率低、绒毡层降解延迟,而雌蕊发育正常,在与野生型的雄性植株杂交后可以成功产生种子。随后作者将pSyGI-SyGI 转基因烟草和FrBy突变体进行正、反杂交,及异源回补FrBy发现SyGI和FrBy独立促进雌蕊和雄蕊的发育(图10)。
图10 FrBy的功能验证(Akagi et al., 2019)。(a-c)在拟南芥中FrBy直系同源物AT1G30800的敲除突变体的表型(a),突变体发育中的花药没有出现绒毡层退化(b),而野生型拟南芥(Col-0)显示绒毡层细胞和成熟小孢子(MS)完全退化(c)。TP:绒毡层细胞,OL:外层,ML,中层;(d、e)突变体(d)和Col-0(e)相比,种子产量降低。SS:没有种子的不育角果,Si:角果;(f)突变体自花授粉和异花授粉后的角果发育,只有与Col-0对照植物进行异花授粉才能产生种子;(g)突变体与Col-0中的花粉发芽率;(h–j)在烟草中,FrBy直系同源物FAS1a/b的敲除突变体表型。An:花药,Sg:柱头,Pe:花瓣;(l、k)与野生型(l)相比,fas1突变体(k)的花粉萌发能力显著降低。Po:花粉粒,PT:花粉管;(m、n)突变体(m)的小孢子阶段,花药解剖后观察到厚的绒毡层,而野生型绒毡层细胞完全退化(n);(o)与突变体相比,SyGI 对花粉萌发率没有显著影响;(p)野生型、突变体和SyGI 表达系的正反杂交表明,FAS1和SyGI 分别仅对雄性和雌性功能起作用;(q、r)异源回补FrBy基因(pFrBy-FrBy)可弥补突变体雄性功能缺失。