本文内容速览:
提到“记忆”这个词,我们通常会首先联想到这种动物大脑或神经系统的能力。
那么问题来了,植物是否也具备记忆能力?动物的记忆依赖于大脑和神经元的突触可塑性,植物虽然没有大脑,却能通过遗传、化学和电信号等方式“记住”外界的信息。事实上,大自然中的诸多现象早已揭示了植物也存在记忆,例如植物在进化过程中对环境的适应——基因组层面的“记忆”让植物能够不断调整自身,以适应复杂多变的外界环境,并得以延续和进化。
相比动物,植物的记忆机制或许更为简单,那有没有一种更通俗的方式来解释植物的记忆过程呢?伯小远认为,植物体内某些物质的持续积累,使其能够长时间保持对特定因素的响应状态,即便脱离了原始环境,这种响应仍然持续存在,这种现象就像植物“记住”了某种环境或环境中的关键因素。
基于这一理解,小远将植物的记忆分为四种类型:表观遗传控制的记忆、信号分子控制的记忆、蛋白控制的记忆以及代谢物控制的记忆。接下来,我们将一起探讨这些不同类型的植物记忆及其对应的案例,希望能帮助大家从“记忆”的角度理解植物的某些生理活动。
表观遗传机制主要包括DNA、RNA和组蛋白的修饰,以及染色质结构和构象的变化。简单来说,表观遗传能够在不改变DNA序列的情况下调控基因表达。Ma和Gallusci等人在综述文章中指出,表观遗传不仅是植物响应外界信号的重要因素,还在植物记忆能力及其“遗忘”能力中发挥关键作用(Ma et al., 2024; Gallusci et al., 2023)。
对于需要春化的植物而言,它们在开花结实之前必须经历一段时间的低温。每一代植物在感受到低温信号后,会“记住”这一经历,而当下一代种子萌发时,这种记忆会被重置,植物需要重新经历春化才能正常开花。那么,植物是如何“记住”和“遗忘”春化的呢?
FLOWERING LOCUS C(FLC)编码一种开花抑制转录因子(该基因高表达抑制开花,低表达则不抑制),在经历春化之前,FLC 基因的染色质上存在H3K4和H3K36三甲基化等激活性修饰,使其维持高水平表达,从而阻碍植物开花(图1A)。在春化处理后,Polycomb蛋白复合体对FLC 染色质进行H3K27三甲基化,这一修饰会抑制FLC的表达(图1B)。有趣的是,即使冬季过去后温度回暖,FLC 染色质的H3K27三甲基化依旧累积。这种情况下,就像植物在温度回暖后仍然会“记得”自己曾经经历过低温,FLC 持续处于抑制,因此植物可以正常开花。
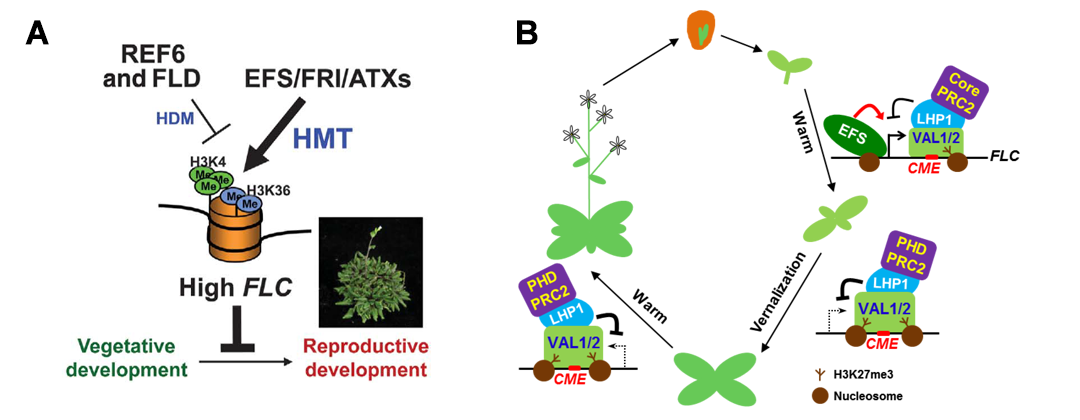 图1 春化前后FLC基因的染色质上表观修饰状态(Ko et al., 2010; Yuan et al., 2016)。(A)春化前H3K4和H3K36三甲基化激活了FLC 的表达,开花受到抑制;(B)纯化后H3K27三甲基化抑制了FLC 的表达,开花抑制缓解。
那么,已经春化过的植物为什么下一代还需要重新春化呢?2022年3月,北京大学现代农业研究院何跃辉课题组在The Plant Cell杂志上发表了一篇题为“Embryonic reactivation of FLOWERING LOCUS C by ABSCISIC ACID-INSENSITIVE 3 establishes the vernalization requirement in each Arabidopsis generation”的研究论文,该研究揭示了植物如何在下一代中丢失春化记忆的分子机制。研究发现,FLC 的再激活分为两个阶段:胚胎发生过程中FLC 沉默状态的去除和胚胎成熟过程中的FLC 激活(图2A)。转录因子ABI3通过结合FLC 基因上的“冷记忆元件(CME)”,招募活性染色质修饰因子,在胚胎晚期将FLC 重置为活跃状态。此外,在胚胎成熟过程中,ABI3还与bZIP转录因子ABI5共同结合ABA响应元件,促进FLC 的高水平表达(图2B)。随着FLC 的重新激活,植物的开花又受到抑制,春化记忆也随之丢失,因此新一代植物需要重新经历低温才能开花。这一研究进一步深化了我们对植物记忆与遗忘机制的理解。
图1 春化前后FLC基因的染色质上表观修饰状态(Ko et al., 2010; Yuan et al., 2016)。(A)春化前H3K4和H3K36三甲基化激活了FLC 的表达,开花受到抑制;(B)纯化后H3K27三甲基化抑制了FLC 的表达,开花抑制缓解。
那么,已经春化过的植物为什么下一代还需要重新春化呢?2022年3月,北京大学现代农业研究院何跃辉课题组在The Plant Cell杂志上发表了一篇题为“Embryonic reactivation of FLOWERING LOCUS C by ABSCISIC ACID-INSENSITIVE 3 establishes the vernalization requirement in each Arabidopsis generation”的研究论文,该研究揭示了植物如何在下一代中丢失春化记忆的分子机制。研究发现,FLC 的再激活分为两个阶段:胚胎发生过程中FLC 沉默状态的去除和胚胎成熟过程中的FLC 激活(图2A)。转录因子ABI3通过结合FLC 基因上的“冷记忆元件(CME)”,招募活性染色质修饰因子,在胚胎晚期将FLC 重置为活跃状态。此外,在胚胎成熟过程中,ABI3还与bZIP转录因子ABI5共同结合ABA响应元件,促进FLC 的高水平表达(图2B)。随着FLC 的重新激活,植物的开花又受到抑制,春化记忆也随之丢失,因此新一代植物需要重新经历低温才能开花。这一研究进一步深化了我们对植物记忆与遗忘机制的理解。
 图2 植物春化后子代春化记忆丢失示意图(He et al., 2022)。(A)植物春化后,FLC 再激活的模式图;(B)冷记忆元件CME招募活性染色质修饰因子将FLC 重置为激活状态。
实际上,不仅仅是冷信号,植物在应对其他类型的非生物胁迫时,表观遗传修饰同样发挥着重要作用。为了更好地感知和适应外界环境,植物会形成某些由表观遗传机制控制的应激记忆。这种记忆在不利环境消失后仍可持续存在,可能在单个植物体内维持一段时间(体细胞记忆),也可能通过种子传递给后代(跨代记忆)(Ma et al., 2024)。
既然表观遗传修饰可以调控植物的记忆,那么是否存在非组蛋白修饰调控的植物记忆呢?事实上,早在2019年,中山大学李剑锋课题组就发现,拟南芥在识别病原细菌后,会诱导其几丁质共受体CERK1的胞内近膜区发生磷酸化修饰,使该受体进入持续48小时以上的“警戒”状态。在这一阶段,CERK1能够更快速、更持久地传导几丁质信号,从而赋予植物增强的真菌抗性(图3)。
图2 植物春化后子代春化记忆丢失示意图(He et al., 2022)。(A)植物春化后,FLC 再激活的模式图;(B)冷记忆元件CME招募活性染色质修饰因子将FLC 重置为激活状态。
实际上,不仅仅是冷信号,植物在应对其他类型的非生物胁迫时,表观遗传修饰同样发挥着重要作用。为了更好地感知和适应外界环境,植物会形成某些由表观遗传机制控制的应激记忆。这种记忆在不利环境消失后仍可持续存在,可能在单个植物体内维持一段时间(体细胞记忆),也可能通过种子传递给后代(跨代记忆)(Ma et al., 2024)。
既然表观遗传修饰可以调控植物的记忆,那么是否存在非组蛋白修饰调控的植物记忆呢?事实上,早在2019年,中山大学李剑锋课题组就发现,拟南芥在识别病原细菌后,会诱导其几丁质共受体CERK1的胞内近膜区发生磷酸化修饰,使该受体进入持续48小时以上的“警戒”状态。在这一阶段,CERK1能够更快速、更持久地传导几丁质信号,从而赋予植物增强的真菌抗性(图3)。
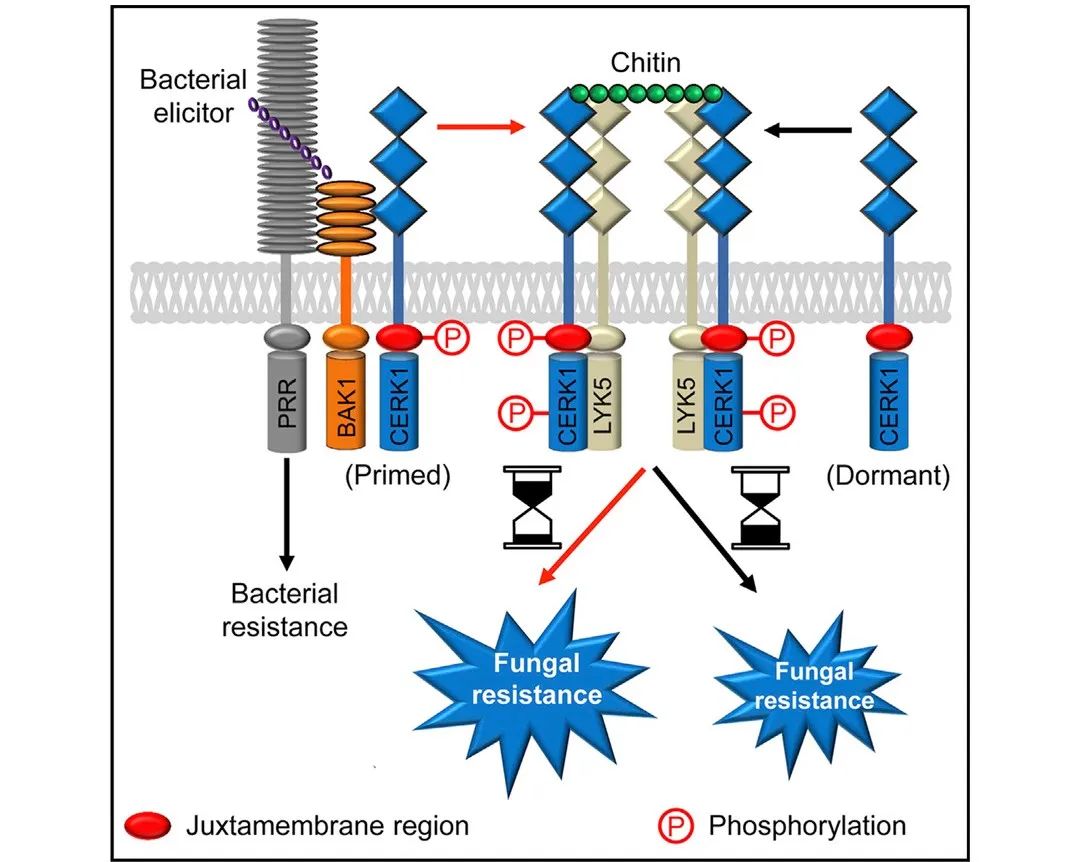 图3 拟南芥识别病原细菌后CERK1处于“警戒”状态(Gong et al., 2019)。
回顾这项研究,我们可以发现,所谓的“警戒”状态,就是在植物没有感知到病原真菌时就保持响应的预备状态,实际上正符合我们对于植物记忆的定义!这表明植物的记忆不仅依赖于经典的表观遗传修饰,如DNA甲基化或组蛋白修饰,非组蛋白修饰(如蛋白质磷酸化)同样可以赋予植物短期甚至长期的环境适应能力。
植物体内存在多种信号分子,如钙离子(Ca²⁺)信号、活性氧(ROS)信号、电信号和激素信号等。这些信号或短暂瞬时,或可持续存在,并通过不同的调控机制精细调节植物的各项生理活动。那么,既然某些信号可以持续存在,是否意味着植物能够通过特定的信号分子实现记忆功能呢?
先前的研究表明,捕蝇草的记忆机制与细胞内Ca²⁺浓度的动态变化密切相关。在触发捕蝇反应的过程中,Ca²⁺浓度的上升是关键因素。只有两次连续的刺激激活Ca²⁺到阈值时,才能真正引发叶片闭合(Hodick and Sievers, 1988)。从以上的研究中我们可以猜测,是否是因为捕蝇草记住了第一次的刺激(可能是Ca²⁺浓度维持在一个高于接受刺激前的水平),才能在第二次刺激时触发捕蝇反应呢?进一步研究发现,单次动作电位(AP)的刺激缺失不足以使细胞质Ca²⁺浓度达到阈值,至少需要两次动作电位的累积效应才能成功触发捕蝇反应。此外,在接受第一次刺激后,细胞质Ca²⁺浓度会逐渐降低,若间隔超过30秒,即使再次受到刺激,Ca²⁺浓度也难以恢复至阈值,导致捕蝇反应无法发生(Jan et al., 2020)。这些研究表明,捕蝇草的捕食行为是一种短期记忆。
然而,由于缺乏能够在捕蝇草体内实时监测Ca²⁺时空动态变化的有效手段,该记忆机制一直未能得到直接验证。2020年10月,日本国立基础生物学研究所Mitsuyasu Hasebe课题组在Nature Plants杂志上发表了一篇题为“Calcium dynamics during trap closure visualized in transgenic Venus flytrap”的研究论文,该研究团队构建了一种组成型表达钙传感蛋白GCaMP6f的载体,该蛋白包含荧光标记部分cpEGFP。通过基因转化将该载体导入捕蝇草体内后,研究人员可以利用荧光信号的变化直观呈现Ca²⁺的动态波动。实验结果进一步验证了先前的结论:捕蝇草叶片的闭合需要短时间内连续两次刺激,第一次刺激后Ca²⁺浓度能够积累,当第二次刺激后,Ca²⁺浓度继续升高达到阈值,叶片闭合。如果两次刺激的时间间隔过长,Ca²⁺浓度无法积累至阈值,叶片将不会闭合(图4)。
该研究通过实时荧光监测手段,为捕蝇草的短期记忆提供了直观的实验证据,也进一步揭示了植物信号调控与记忆功能之间的关联。另外,关于荧光蛋白作为离子传感器的详细信息,可以查看小远之前写的文章“荧光蛋白的升级用法”。
图3 拟南芥识别病原细菌后CERK1处于“警戒”状态(Gong et al., 2019)。
回顾这项研究,我们可以发现,所谓的“警戒”状态,就是在植物没有感知到病原真菌时就保持响应的预备状态,实际上正符合我们对于植物记忆的定义!这表明植物的记忆不仅依赖于经典的表观遗传修饰,如DNA甲基化或组蛋白修饰,非组蛋白修饰(如蛋白质磷酸化)同样可以赋予植物短期甚至长期的环境适应能力。
植物体内存在多种信号分子,如钙离子(Ca²⁺)信号、活性氧(ROS)信号、电信号和激素信号等。这些信号或短暂瞬时,或可持续存在,并通过不同的调控机制精细调节植物的各项生理活动。那么,既然某些信号可以持续存在,是否意味着植物能够通过特定的信号分子实现记忆功能呢?
先前的研究表明,捕蝇草的记忆机制与细胞内Ca²⁺浓度的动态变化密切相关。在触发捕蝇反应的过程中,Ca²⁺浓度的上升是关键因素。只有两次连续的刺激激活Ca²⁺到阈值时,才能真正引发叶片闭合(Hodick and Sievers, 1988)。从以上的研究中我们可以猜测,是否是因为捕蝇草记住了第一次的刺激(可能是Ca²⁺浓度维持在一个高于接受刺激前的水平),才能在第二次刺激时触发捕蝇反应呢?进一步研究发现,单次动作电位(AP)的刺激缺失不足以使细胞质Ca²⁺浓度达到阈值,至少需要两次动作电位的累积效应才能成功触发捕蝇反应。此外,在接受第一次刺激后,细胞质Ca²⁺浓度会逐渐降低,若间隔超过30秒,即使再次受到刺激,Ca²⁺浓度也难以恢复至阈值,导致捕蝇反应无法发生(Jan et al., 2020)。这些研究表明,捕蝇草的捕食行为是一种短期记忆。
然而,由于缺乏能够在捕蝇草体内实时监测Ca²⁺时空动态变化的有效手段,该记忆机制一直未能得到直接验证。2020年10月,日本国立基础生物学研究所Mitsuyasu Hasebe课题组在Nature Plants杂志上发表了一篇题为“Calcium dynamics during trap closure visualized in transgenic Venus flytrap”的研究论文,该研究团队构建了一种组成型表达钙传感蛋白GCaMP6f的载体,该蛋白包含荧光标记部分cpEGFP。通过基因转化将该载体导入捕蝇草体内后,研究人员可以利用荧光信号的变化直观呈现Ca²⁺的动态波动。实验结果进一步验证了先前的结论:捕蝇草叶片的闭合需要短时间内连续两次刺激,第一次刺激后Ca²⁺浓度能够积累,当第二次刺激后,Ca²⁺浓度继续升高达到阈值,叶片闭合。如果两次刺激的时间间隔过长,Ca²⁺浓度无法积累至阈值,叶片将不会闭合(图4)。
该研究通过实时荧光监测手段,为捕蝇草的短期记忆提供了直观的实验证据,也进一步揭示了植物信号调控与记忆功能之间的关联。另外,关于荧光蛋白作为离子传感器的详细信息,可以查看小远之前写的文章“荧光蛋白的升级用法”。
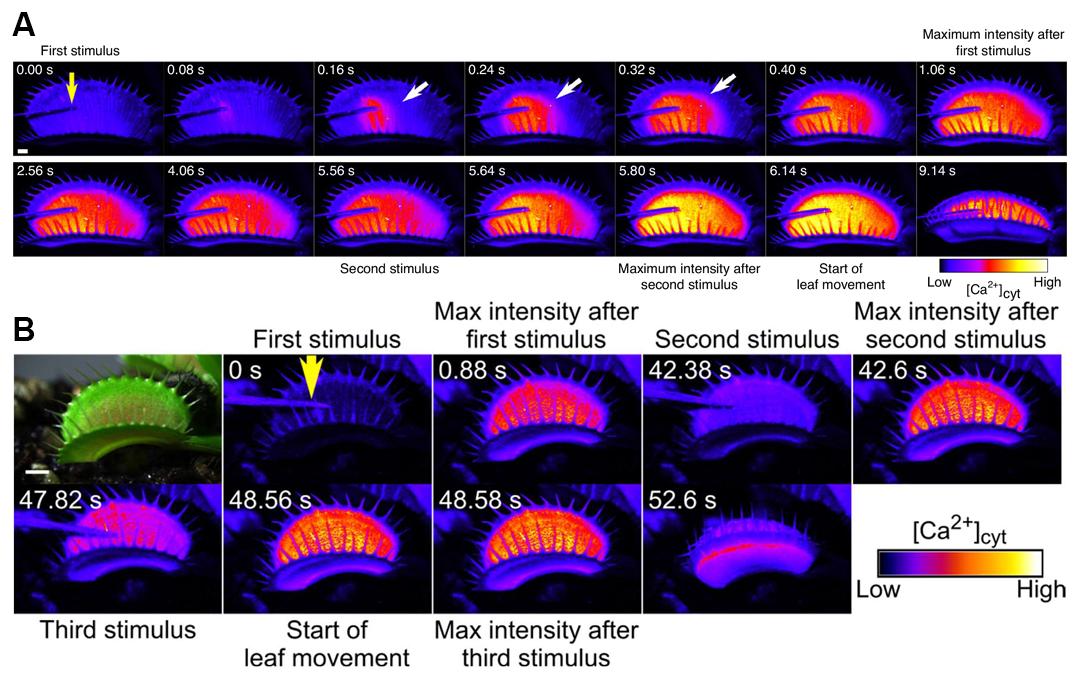 图4 捕蝇草在接受不同时间间隔刺激后的Ca²⁺浓度变化及叶片张开/闭合的状态(Suda et al., 2020)。(A)短期内的两次刺激使细胞质Ca²⁺浓度达到阈值从而使捕蝇草闭合;(B)两次较长时间间隔的刺激不能使捕蝇草闭合,紧接着短时间的第三次刺激可以使细胞质Ca²⁺浓度达到阈值,捕蝇草闭合。
图4 捕蝇草在接受不同时间间隔刺激后的Ca²⁺浓度变化及叶片张开/闭合的状态(Suda et al., 2020)。(A)短期内的两次刺激使细胞质Ca²⁺浓度达到阈值从而使捕蝇草闭合;(B)两次较长时间间隔的刺激不能使捕蝇草闭合,紧接着短时间的第三次刺激可以使细胞质Ca²⁺浓度达到阈值,捕蝇草闭合。
除了捕蝇草之外,在日常生活中常见的含羞草也表现出类似的记忆行为。当受到外界刺激时,含羞草的叶片会迅速闭合。然而,在经历多次重复刺激后,叶片的反应逐渐减弱,最终表现出“无动于衷”的状态。更有趣的是,即使在数天后,含羞草依然能够记住先前的刺激经历,并持续表现出这一适应性反应(Monica et al., 2014)。
尽管这类记忆被单独归类,但从本质上来看,某些信号分子(例如某些激素)本身也是代谢物。只不过,在研究这些信号分子时,人们通常不会从代谢物的角度进行理解,而是更多关注其作为信号分子时发挥的作用。因此,出于研究范畴的考虑,仍将这类记忆划分为独立的一类。
蛋白质作为功能的直接行使者,其持续积累也会导致植物处于某种响应状态。2020年10月,霍亨海姆大学Julia课题组联合其他单位在Environmental and Experimental Botany杂志上发表了一篇题为“Plant stress memory is linked to high levels of anti-oxidative enzymes over several weeks”的研究论文,该研究发现,在经过持续干旱和极湿处理后,再经过三周的恢复处理(使植物处于正常的生长环境)后,当再次经历干旱时,之前经历过干旱的植物组织损伤较少,Rubisco(核酮糖-1,5-二磷酸羧化酶)和抗氧化酶(POX、SOD)等含量较高(图5)。这一现象表明,植物能够通过相关蛋白的持续积累,形成对干旱环境的长期记忆,从而提高自身的抗逆能力。
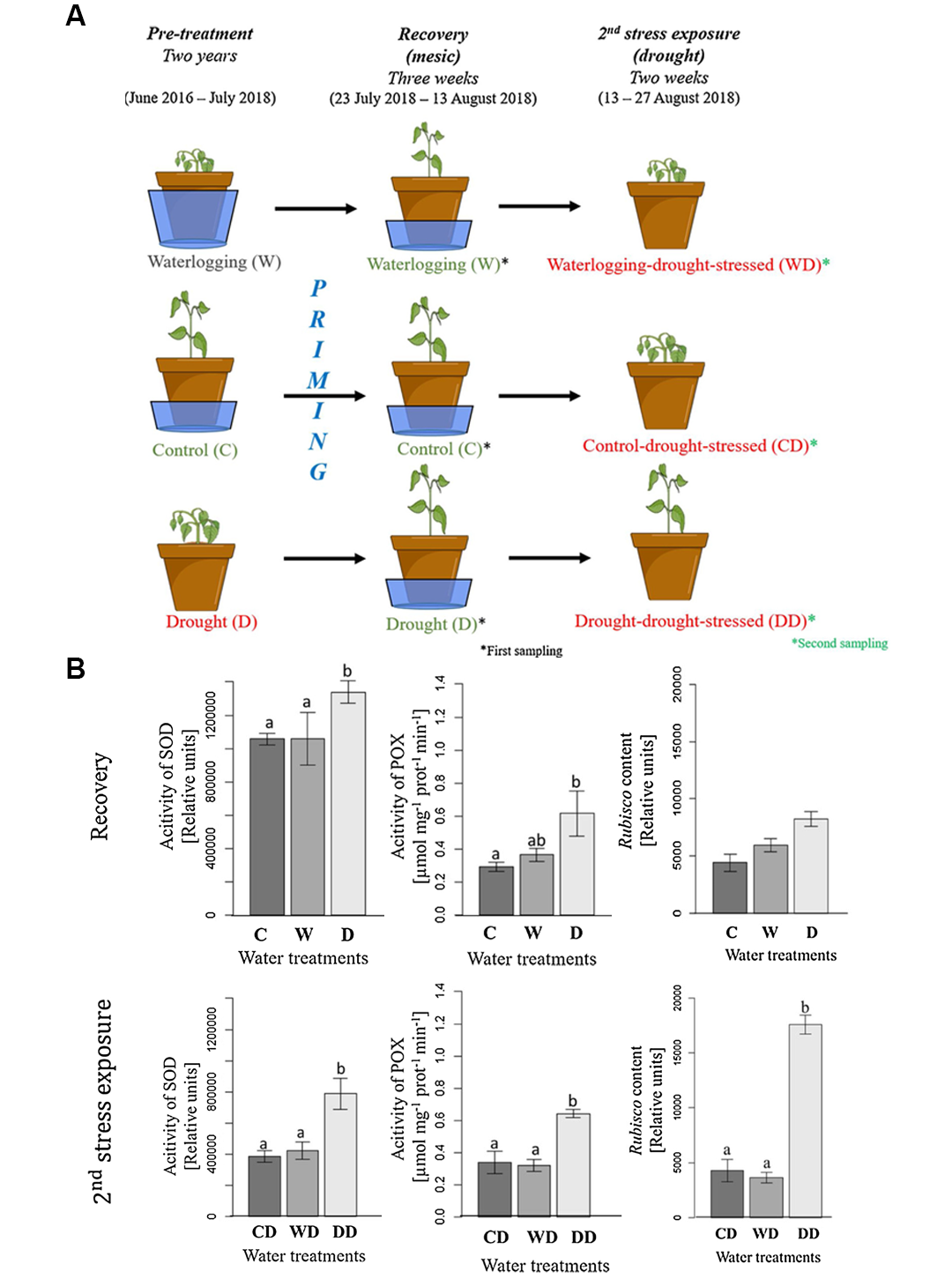 图5 不同处理后植物应对干旱时的表现(Nataša et al., 2020)。(A)不同处理(极湿、对照和干旱)的模式图;(B)不同处理恢复期及后续干旱处理后SOD、POX和Rubisco的含量测定,结果表明,在已经经历过干旱处理的材料中,其SOD、POX和Rubisco的含量在恢复期后持续维持高水平。
在上述研究中,作者虽然发现蛋白质的积累可以赋予植物一定的记忆能力,但其具体机制仍不明确。目前尚不清楚这些蛋白的持续存在仅仅是由于降解受阻,还是其基因表达水平也一直维持在较高状态。如果是后者,那么这一现象可能与表观遗传调控密切相关,应归类为表观遗传控制的记忆。然而,如果暂不考虑蛋白积累背后的具体机制,仅从功能表现来看,将这一现象视作蛋白介导的记忆同样是合理的。
植物体内的代谢物种类繁多,其中一些代谢物不仅被视为信号分子,还在多种生理过程中发挥重要作用。那么,是否存在某些代谢物能够持续积累,从而赋予植物环境记忆呢?提到这一点,小远首先想到的便是植物免疫中的系统性获得抗性(SAR)。当植物的局部组织遭受病原菌侵染后,会通过积累水杨酸(SA)使其他未受侵染的部位提前进入防御状态。显然,在这种情况下,植物“记住”了局部的侵染经历,并在全株范围内激活广谱抗性。
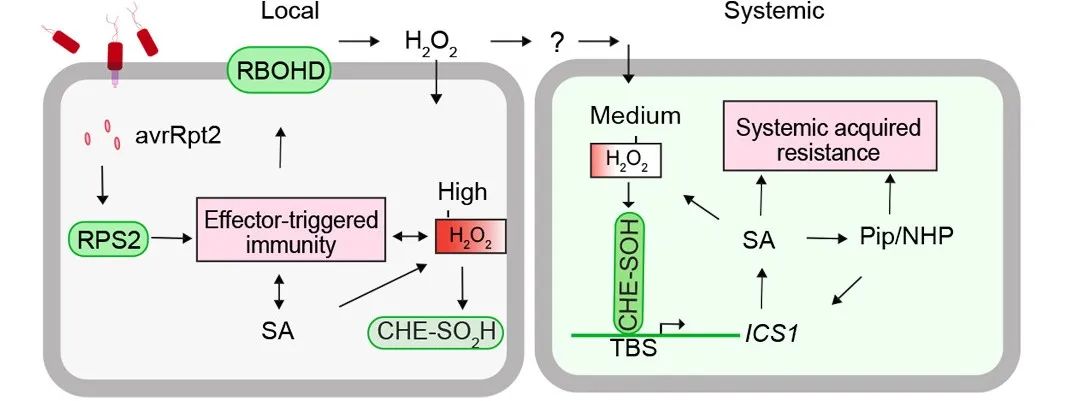
2024年9月,杜克大学董欣年课题组在Science杂志上发表了一篇题为“H2O2 sulfenylates CHE, linking local infection to establishment of systemic acquired resistance”的研究论文,该研究进一步解析了SA为何能在未受侵染部位积累的机制。研究发现,过氧化氢(H2O2)能够从受感染部位传导至健康组织,并在那里诱导生物钟基因蛋白CCA1 Hiking Expedition(CHE)发生巯基化修饰(-SOH)。巯基化后的CHE增强了其对水杨酸合成关键基因ICS1启动子的结合能力,从而促进ICS1的表达,最终诱导SA的合成并触发系统性获得抗性(图6)。
这一研究不仅揭示了植物如何在全株范围内建立免疫记忆,也进一步阐明了代谢物在植物记忆机制中的核心作用。
图6 过氧化氢介导植物未受病原菌侵染部位的SA合成从而使植物表现出获得性抗性(Dong et al., 2024)。
除了水杨酸(SA)之外,其他植物激素如乙烯同样在植物的生理活动和环境适应过程中发挥着重要作用。当这些激素信号持续积累时,植物便能表现出对环境的记忆。
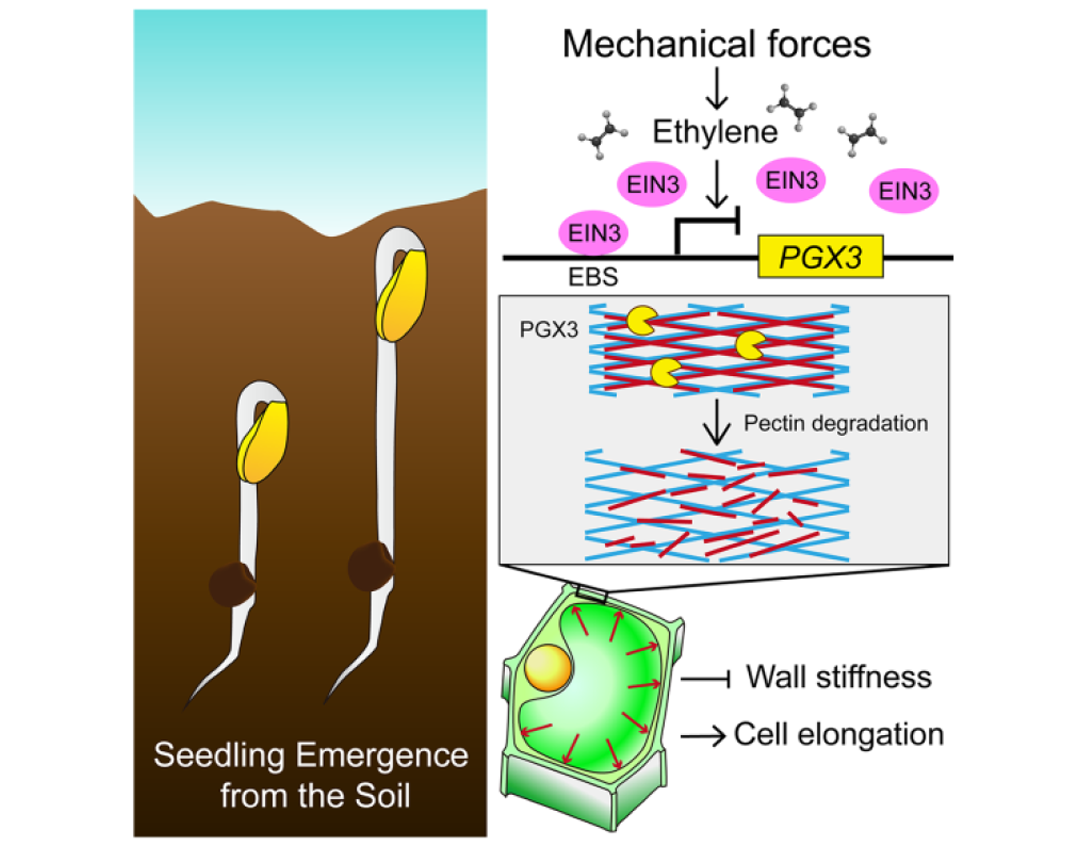
例如,北京大学钟上威课题组的研究发现,持续的机械压力会导致植物积累乙烯信号,从而影响其生长适应性。在这一过程中,乙烯信号通路的关键转录因子EIN3在感受到乙烯信号后,会直接结合并抑制PGX3基因的表达。PGX3在果胶的水解过程中起重要作用,其表达受抑制后,植物的细胞壁特性发生变化,使幼苗能够更好地适应外界压力(图7)。最终,植物记住了机械压力的影响,调整自身生长策略,提高成功出土的存活率。
图7 持续的机械压力使植物合成乙烯记住压力信号(Zhong et al., 2020)。
这一研究进一步表明,植物激素信号的持续积累不仅调控生长发育,还在环境适应性记忆中发挥关键作用。基于这一点,该论文作者也在文中提到,几百年来农民一直使用机械刺激处理来强化植物茎秆,例如故意踩踏小麦和大麦幼苗或将小鸭子放入稻田中。因此,这种适应性记忆可以在未来进一步指导农业生产,在减少化学农药使用的同时让农作物健康茁壮地成长。
植物的记忆过程本质上是分子的积累,但如果这些分子在发挥作用后通常会被降解,那么这种积累是如何维持的?它完全由遗传决定,还是受到环境的调控?植物记忆是一种在遗传背景下,由环境触发的动态调控过程。这可能涉及表观遗传修饰、信号分子、相关蛋白及修饰以及代谢物的积累(可能是由于这些分子受到某些调控导致降解过程较慢,因此短时间内依旧积累),使植物即使在未遭遇胁迫时,也能保持一定的应对能力,而非每次都从零开始。
传统的分子研究时常用模式图简化植物生命活动,将其描述为单一或几个信号的激活与抑制。然而,植物的记忆并非单纯的信号传递,而是一种持续的分子状态(即某些物质的持续积累),使其能够未雨绸缪,而非被动响应。这种现象超越了简单的线性因果关系,更像是一种动态适应策略。
从实际应用来看,以记忆的角度研究植物,不仅能深化我们对其生理机制的理解,还能为农业提供新思路。如果能够利用植物的记忆机制,让作物在胁迫到来前就建立适应性,就可能提升其抗逆性、优化表型,并减少对化学农药的依赖。这为作物育种和可持续农业发展提供了新的可能性。
Burri J T, Saikia E, Läubli N F, et al. A single touch can provide sufficient mechanical stimulation to trigger Venus flytrap closure[J]. PLoS biology, 2020, 18(7): e3000740.
Cao L, Karapetyan S, Yoo H, et al. H2O2 sulfenylates CHE, linking local infection to the establishment of systemic acquired resistance[J]. Science, 2024, 385(6714): 1211-1217.
Gagliano M, Renton M, Depczynski M, et al. Experience teaches plants to learn faster and forget slower in environments where it matters[J]. Oecologia, 2014, 175: 63-72.
Gallusci P, Agius D R, Moschou P N, et al. Deep inside the epigenetic memories of stressed plants[J]. Trends in Plant Science, 2023, 28(2): 142-153.
Gong B Q, Guo J, Zhang N, et al. Cross-microbial protection via priming a conserved immune co-receptor through juxtamembrane phosphorylation in plants[J]. Cell host & microbe, 2019, 26(6): 810-822. e7.
Hodick D, Sievers A. The action potential of Dionaea muscipula Ellis[J]. Planta, 1988, 174: 8-18.
Ko J H, Mitina I, Tamada Y, et al. Growth habit determination by the balance of histone methylation activities in Arabidopsis[J]. The EMBO journal, 2010, 29(18): 3208-3215.
Ma L, Xing L, Li Z, et al. Epigenetic control of plant abiotic stress responses[J]. Journal of Genetics and Genomics, 2024.
Suda H, Mano H, Toyota M, et al. Calcium dynamics during trap closure visualized in transgenic Venus flytrap[J]. Nature Plants, 2020, 6(10): 1219-1224.
Wu Q, Li Y, Lyu M, et al. Touch-induced seedling morphological changes are determined by ethylene-regulated pectin degradation[J]. Science advances, 2020, 6(48): eabc9294.
Xu G, Tao Z, He Y. Embryonic reactivation of FLOWERING LOCUS C by ABSCISIC ACID-INSENSITIVE 3 establishes the vernalization requirement in each Arabidopsis generation[J]. The Plant Cell, 2022, 34(6): 2205-2221.
Yuan W, Luo X, Li Z, et al. A cis cold memory element and a trans epigenome reader mediate Polycomb silencing of FLC by vernalization in Arabidopsis[J]. Nature genetics, 2016, 48(12): 1527-1534.
图5 不同处理后植物应对干旱时的表现(Nataša et al., 2020)。(A)不同处理(极湿、对照和干旱)的模式图;(B)不同处理恢复期及后续干旱处理后SOD、POX和Rubisco的含量测定,结果表明,在已经经历过干旱处理的材料中,其SOD、POX和Rubisco的含量在恢复期后持续维持高水平。
在上述研究中,作者虽然发现蛋白质的积累可以赋予植物一定的记忆能力,但其具体机制仍不明确。目前尚不清楚这些蛋白的持续存在仅仅是由于降解受阻,还是其基因表达水平也一直维持在较高状态。如果是后者,那么这一现象可能与表观遗传调控密切相关,应归类为表观遗传控制的记忆。然而,如果暂不考虑蛋白积累背后的具体机制,仅从功能表现来看,将这一现象视作蛋白介导的记忆同样是合理的。
植物体内的代谢物种类繁多,其中一些代谢物不仅被视为信号分子,还在多种生理过程中发挥重要作用。那么,是否存在某些代谢物能够持续积累,从而赋予植物环境记忆呢?提到这一点,小远首先想到的便是植物免疫中的系统性获得抗性(SAR)。当植物的局部组织遭受病原菌侵染后,会通过积累水杨酸(SA)使其他未受侵染的部位提前进入防御状态。显然,在这种情况下,植物“记住”了局部的侵染经历,并在全株范围内激活广谱抗性。
2024年9月,杜克大学董欣年课题组在Science杂志上发表了一篇题为“H2O2 sulfenylates CHE, linking local infection to establishment of systemic acquired resistance”的研究论文,该研究进一步解析了SA为何能在未受侵染部位积累的机制。研究发现,过氧化氢(H2O2)能够从受感染部位传导至健康组织,并在那里诱导生物钟基因蛋白CCA1 Hiking Expedition(CHE)发生巯基化修饰(-SOH)。巯基化后的CHE增强了其对水杨酸合成关键基因ICS1启动子的结合能力,从而促进ICS1的表达,最终诱导SA的合成并触发系统性获得抗性(图6)。
这一研究不仅揭示了植物如何在全株范围内建立免疫记忆,也进一步阐明了代谢物在植物记忆机制中的核心作用。
图6 过氧化氢介导植物未受病原菌侵染部位的SA合成从而使植物表现出获得性抗性(Dong et al., 2024)。
除了水杨酸(SA)之外,其他植物激素如乙烯同样在植物的生理活动和环境适应过程中发挥着重要作用。当这些激素信号持续积累时,植物便能表现出对环境的记忆。
例如,北京大学钟上威课题组的研究发现,持续的机械压力会导致植物积累乙烯信号,从而影响其生长适应性。在这一过程中,乙烯信号通路的关键转录因子EIN3在感受到乙烯信号后,会直接结合并抑制PGX3基因的表达。PGX3在果胶的水解过程中起重要作用,其表达受抑制后,植物的细胞壁特性发生变化,使幼苗能够更好地适应外界压力(图7)。最终,植物记住了机械压力的影响,调整自身生长策略,提高成功出土的存活率。
图7 持续的机械压力使植物合成乙烯记住压力信号(Zhong et al., 2020)。
这一研究进一步表明,植物激素信号的持续积累不仅调控生长发育,还在环境适应性记忆中发挥关键作用。基于这一点,该论文作者也在文中提到,几百年来农民一直使用机械刺激处理来强化植物茎秆,例如故意踩踏小麦和大麦幼苗或将小鸭子放入稻田中。因此,这种适应性记忆可以在未来进一步指导农业生产,在减少化学农药使用的同时让农作物健康茁壮地成长。
植物的记忆过程本质上是分子的积累,但如果这些分子在发挥作用后通常会被降解,那么这种积累是如何维持的?它完全由遗传决定,还是受到环境的调控?植物记忆是一种在遗传背景下,由环境触发的动态调控过程。这可能涉及表观遗传修饰、信号分子、相关蛋白及修饰以及代谢物的积累(可能是由于这些分子受到某些调控导致降解过程较慢,因此短时间内依旧积累),使植物即使在未遭遇胁迫时,也能保持一定的应对能力,而非每次都从零开始。
传统的分子研究时常用模式图简化植物生命活动,将其描述为单一或几个信号的激活与抑制。然而,植物的记忆并非单纯的信号传递,而是一种持续的分子状态(即某些物质的持续积累),使其能够未雨绸缪,而非被动响应。这种现象超越了简单的线性因果关系,更像是一种动态适应策略。
从实际应用来看,以记忆的角度研究植物,不仅能深化我们对其生理机制的理解,还能为农业提供新思路。如果能够利用植物的记忆机制,让作物在胁迫到来前就建立适应性,就可能提升其抗逆性、优化表型,并减少对化学农药的依赖。这为作物育种和可持续农业发展提供了新的可能性。
Burri J T, Saikia E, Läubli N F, et al. A single touch can provide sufficient mechanical stimulation to trigger Venus flytrap closure[J]. PLoS biology, 2020, 18(7): e3000740.
Cao L, Karapetyan S, Yoo H, et al. H2O2 sulfenylates CHE, linking local infection to the establishment of systemic acquired resistance[J]. Science, 2024, 385(6714): 1211-1217.
Gagliano M, Renton M, Depczynski M, et al. Experience teaches plants to learn faster and forget slower in environments where it matters[J]. Oecologia, 2014, 175: 63-72.
Gallusci P, Agius D R, Moschou P N, et al. Deep inside the epigenetic memories of stressed plants[J]. Trends in Plant Science, 2023, 28(2): 142-153.
Gong B Q, Guo J, Zhang N, et al. Cross-microbial protection via priming a conserved immune co-receptor through juxtamembrane phosphorylation in plants[J]. Cell host & microbe, 2019, 26(6): 810-822. e7.
Hodick D, Sievers A. The action potential of Dionaea muscipula Ellis[J]. Planta, 1988, 174: 8-18.
Ko J H, Mitina I, Tamada Y, et al. Growth habit determination by the balance of histone methylation activities in Arabidopsis[J]. The EMBO journal, 2010, 29(18): 3208-3215.
Ma L, Xing L, Li Z, et al. Epigenetic control of plant abiotic stress responses[J]. Journal of Genetics and Genomics, 2024.
Suda H, Mano H, Toyota M, et al. Calcium dynamics during trap closure visualized in transgenic Venus flytrap[J]. Nature Plants, 2020, 6(10): 1219-1224.
Wu Q, Li Y, Lyu M, et al. Touch-induced seedling morphological changes are determined by ethylene-regulated pectin degradation[J]. Science advances, 2020, 6(48): eabc9294.
Xu G, Tao Z, He Y. Embryonic reactivation of FLOWERING LOCUS C by ABSCISIC ACID-INSENSITIVE 3 establishes the vernalization requirement in each Arabidopsis generation[J]. The Plant Cell, 2022, 34(6): 2205-2221.
Yuan W, Luo X, Li Z, et al. A cis cold memory element and a trans epigenome reader mediate Polycomb silencing of FLC by vernalization in Arabidopsis[J]. Nature genetics, 2016, 48(12): 1527-1534.