近日,Plant Biotechnology Journal在线发表了由西北农林科技大学园艺学院王跃进教授课题组撰写的“VqERF1B-VqERF062-VqNSTS2 transcriptional cascade enhances stilbene biosynthesis and resistance to powdery mildew in grape”论文。依据前期在中国野生毛葡萄‘丹凤-2’中通过转录组数据分析发现的一个新的基因VqNSTS2,此项研究对VqNSTS2结构特征分析,瞬时转入模式植物烟草中检测到其表达芪类产物以及其在‘丹凤-2’人工接种葡萄白粉病菌条件下表达了抗病性;将中国野生葡萄芪合酶基因VqNSTS2稳定转化至拟南芥和感病葡萄中,在拟南芥接种白粉病菌后,发现了VqNSTS2在白粉菌入侵时通过聚集到真菌孢子的吸器处,阻止孢子进一步入侵从而增强植株对白粉菌的抗性。通过多种体内、体外互作方法研究,揭示了VqERF062除了能自身形成同源二聚体外,还可与VqERF1B形成异源二聚体,协同促进对VqNSTS2的转录调控,增强葡萄对白粉病的抗性。该研究成果揭示了中国野生毛葡萄VqERF1B-VqERF062蛋白复合体增强VqNSTS2的表达及其调控葡萄抗白粉病的分子机制,为葡萄抗病分子育种提供了重要的基因资源和理论基础,对推动葡萄抗病品种培育具有重要意义。
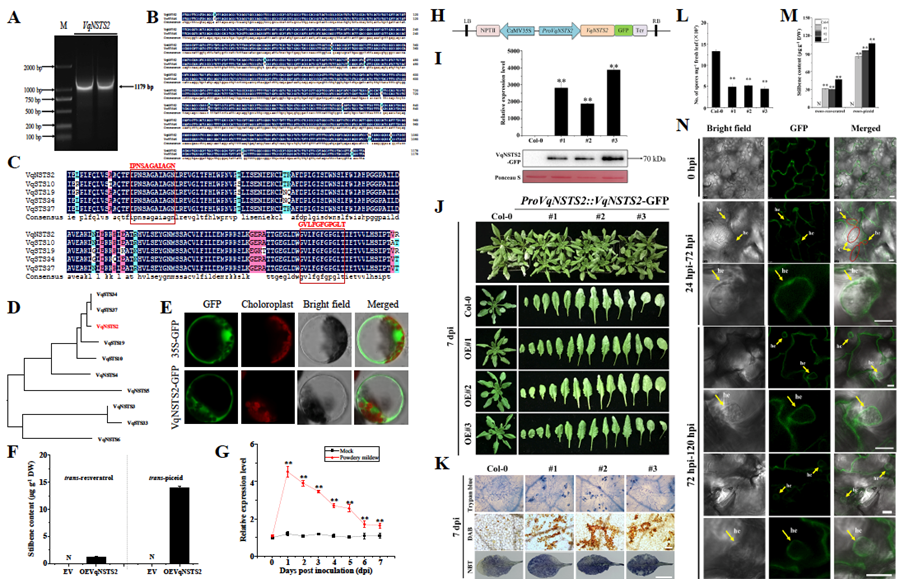
新基因VqNSTS2结构特征分析,瞬时转入模式植物烟草中检测到其表达芪类产物,在’丹凤-2’人工接种白粉病菌后表达了抗病性(图1A-G);拟南芥作为本身不含芪类物质的植物,是研究芪合成酶基因功能的理想选择。研究者将前期筛选获得的中国野生毛葡萄中VqNSTS2基因转入拟南芥中进行抗病功能研究。在接种拟南芥白粉菌(Golovinomyces cichoracearum)后,ProVqNSTS2::VqNSTS2稳定转化的拟南芥植株出现过敏性细胞坏死现象并积累较多的H2O2,同时检测到芪类物质的合成(图1H-M);特别是通过激光共聚焦显微镜观察发现,芪合成酶VqNSTS2经囊泡转运至拟南芥白粉病菌孢子的吸器处,包裹吸器形成吸器鞘,从而抵抗阻挡白粉菌的入侵(图1N)。上述结果表明,VqNSTS2可通过促进芪类物质积累和包裹真菌孢子吸器增强植物对白粉菌的抗性。
图1VqNSTS2基因增强植株对白粉菌的抗性
为了进一步研究新基因VqNSTS2的抗病功能,研究者利用农杆菌介导的转基因再生体系,将VqNSTS2转入不抗病的欧洲葡萄品种‘无核白’中,获得了VqNSTS2穏转过表达的转基因葡萄株系,在人工接种葡萄白粉病菌后发现,转基因葡萄植株中芪类物质含量显著增加,而且促进了防御相关基因的表达,最终增强葡萄了对白粉病的抗性(图2A-I)。与之相反,利用RANi技术在中国野生毛葡萄‘丹凤-2’中瞬时沉默VqNSTS2,接种白粉菌后发现芪类物质含量、防御相关基因的表达等均显著低于对照,孢子数显著高于对照,说明VqNSTS2被干扰后的葡萄叶片对白粉菌的敏感性增强(图2J-P)。以上结果表明,VqNSTS2应答白粉病菌后,可以通过促进芪类物质的积累和防御相关基因的表达增强葡萄对白粉病的抗性。
图2VqNSTS2基因增强对葡萄白粉菌的抗性
基于葡萄叶片接菌前后的转录组数据,通过共表达分析,筛选获得一个可能参与调控VqNSTS2表达的ERF转录因子VqERF062。为了证实VqERF062对VqNSTS2的调控关系,研究者利用Y1H、LUC和EMSA实验证明了VqERF062可以直接结合VqNSTS2启动子上的DRE和RAA元件,激活VqNSTS2基因的表达(图3A-E)。此外,研究者在‘丹凤-2’叶片中瞬时表达VqERF062,通过检测VqNSTS2基因的表达和芪类物质的含量,进一步证明了VqERF062可以激活VqNSTS2基因的表达从而产生更多的芪类物质(图3F-H)。以上结果表明,VqERF062直接结合VqNSTS2启动子上的DRE和RAA元件,激活VqNSTS2的表达促进芪类物质的积累。
图3VqERF062促进VqNSTS2的表达和芪类物质的积累
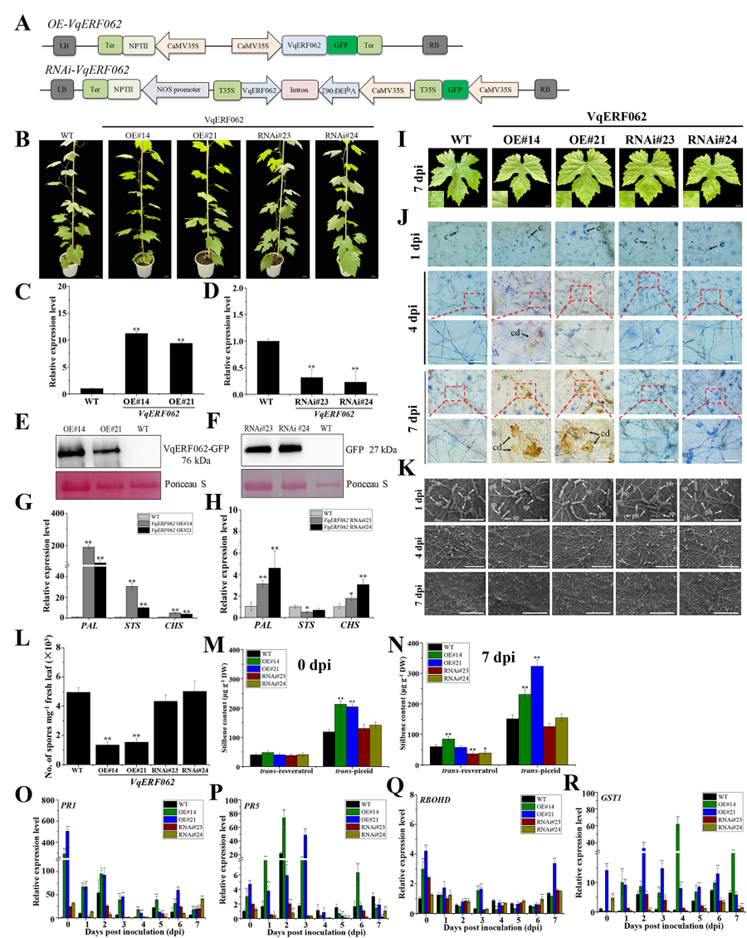
为了进一步探究VqERF062在抗白粉病过程中的作用,研究者采用农杆菌介导的葡萄遗传转化,创制了VqERF062的稳定过表达和干扰株系(图4A-F)。结果发现,在VqERF062过表达株系中,STS的表达量显著增加,反之在干扰株系中STS的表达量降低。随后,研究者对VqERF062转基因葡萄株系接种葡萄白粉菌,发现VqERF062过表达株系积累了较多的芪类物质,表现了更为明显的过敏性细胞坏死现象,防御相关基因显著上调表达,而且真菌孢子数显著降低、菌丝生长缓慢(图4L-R)。但是在干扰株系中却出现相反的结果(图4L-R)。以上结果表明,VqERF062可以通过促进芪类物质的积累和防御相关基因的表达增强葡萄对白粉菌的抗性。
图4VqERF062增强葡萄对白粉菌的抗性
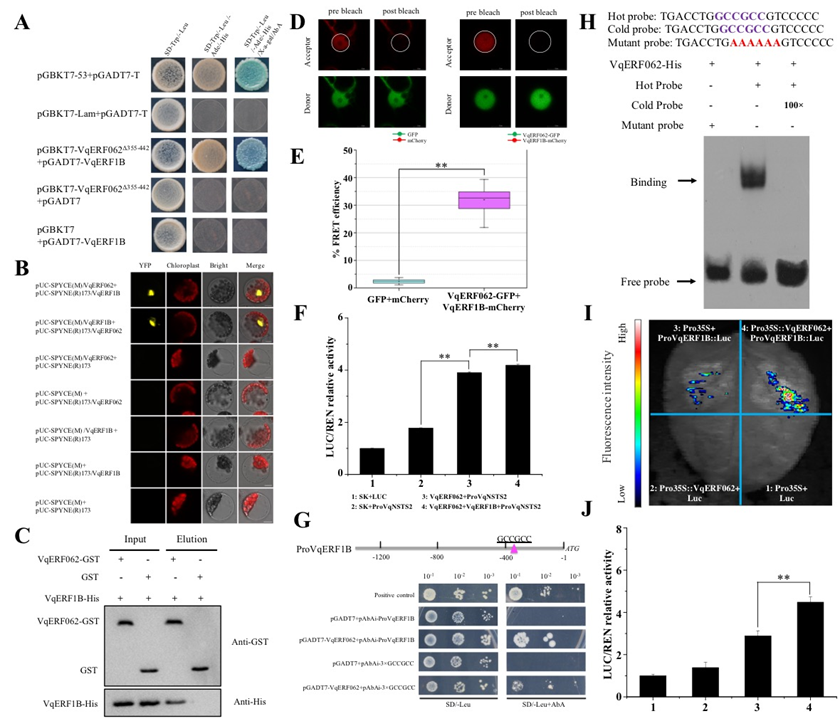
为了进一步探究VqERF062-VqNSTS2参与调控植物对白粉菌抗性的调控机制,研究者利用在线分析工具VTCdb(https://arxiv.org/abs/1305.2083v1)预测了VqERF062的候选互作蛋白。进一步通过Y2H、Co-IP、Pull-down和FRET实验证明了VqERF062可以与VqERF1B发生互作(图5A-E)。为了探究VqERF062与VqERF1B互作后是否对VqNSTS2的调控产生了影响,研究者利用双荧光素酶试验,发现VqERF062与VqERF1B互作后促进了对VqNSTS2的调控表达(图5F)。为进一步深入研究VqERF062与VqERF1B之间的关系,研究者克隆了VqERF1B的启动子序列,发现在VqERF1B的启动子上存在ERF的结合位点,GCC-box(图5G)。因此,研究者利用Y1H、EMSA和LUC实验研究了VqERF062是否直接调控VqERF1B的表达。结果表明VqERF062可以直接结合VqERF1B的启动子上的GCC-box元件(图5G-J)。此外,为了探究VqERF062是否可以以同源二聚体的蛋白形式发挥转录调控功能,研究者进行了Y2H、Co-IP和Pull-down实验,结果表明VqERF062可以与自身发生互作形成同源二聚体。以上结果表明,VqERF062以成同源二聚体以及VqERF062-VqERF1B蛋白复合体协同调控VqNSTS2基因的表达。
图5VqERF1B-VqERF062蛋白复合体协同调控VqNSTS2基因的表达
https://onlinelibrary.wiley.com/doi/10.1111/pbi.70041
References:
Hain R, Reif HJR, Krause E, Langebartels R, Kindl H, Vornam B, Wiese W, Schmelzer E, Schreier PH, Stöcker RH (1993) Disease resistance results from foreign phytoalexin expression in a novel plant. Nature 361 (6408):153-156
Höll J, Vannozzi A, Czemmel S, D’Onofrio C, Walker AR, Rausch T, Lucchin M, Boss PK, Dry IB, Bogs J (2013) The R2R3-MYB transcription factors MYB14 and MYB15 regulate stilbene biosynthesis in Vitis vinifera. Plant Cell 25 (10):4135-4149
Hu Y, Cheng Y, Yu X, Liu J, Yang L, Gao Y, Ke G, Zhou M, Mu B, Xiao S, Wang Y, Wen Y-Q (2021) Overexpression of two CDPKs from wild Chinese grapevine enhances powdery mildew resistance in Vitis vinifera and Arabidopsis. New Phytologist 230 (5):2029-2046
Jang MS, Cai L, Udeani GO, Slowing KV, Pezzuto JM (1997) Cancer Chemopreventive Activity of Resveratrol, a Natural Product Derived from Grapes. Science 275 (5297):218-220
Jones JDG, Dangl JL (2006) The plant immune system. Nature 444 (7117):323-329.
Li Z, Wu R, Guo F, Wang Y, Nick P, Wang X (2025) Advances in the molecular mechanism of grapevine resistance to fungal diseases. Molecular horticulture 5 (1):1. doi:10.1186/s43897-024-00119-x
Ma F, Wang L, Wang Y (2018) Ectopic expression of VpSTS29, a stilbene synthase gene from Vitis pseudoreticulata, indicates STS presence in cytosolic oil bodies. Planta 248 (1):89-103
Qiu W, Feechan A, Dry I (2015) Current understanding of grapevine defense mechanisms against the biotrophic fungus (Erysiphe necator), the causal agent of powdery mildew disease. Horticulture Research 2:15020
Ramming DW, Gabler F, Smilanick J, Cadle-Davidson M, Barba P, Mahanil S, Cadle-Davidson L (2010) A Single Dominant Locus, Ren4, Confers Rapid Non-Race-Specific Resistance to Grapevine Powdery Mildew. Phytopathology 101 (4):502-508
Shi J, He M, Cao J, Wang H, Ding J, Jiao Y, Li R, He J, Wang D, Wang Y (2014) The comparative analysis of the potential relationship between resveratrol and stilbene synthase gene family in the development stages of grapes (Vitis quinquangularis and Vitis vinifera). Plant Physiology & Biochemistry 74:24-32
Wang Y, Liu Y, P. HE, Chen J, Lamikanra O, Lu J (1995) Evaluation of foliar resistance to Uncinulanecator in Chinese wild Vitis spp. species. Vitis 34 (3):159-164
Xu W, Ma F, Li R, Zhou Q, Yao W, Jiao Y, Zhang C, Zhang J, Wang X, Xu Y, Wang Y (2019a) VpSTS29/STS2 enhances fungal tolerance in grapevine through a positive feedback loop. Plant, Cell & Environment 42 (11):2979-2998
Xu W, Ma F, Li R, Zhou Q, Yao W, Jiao Y, Zhang C, Zhang J, Wang X, Xu Y, Wang Y (2019b) VpSTS29/STS2 enhances fungal tolerance in grapevine through a positive feedback loop. Plant Cell and Environment 42 (11):2979-2998
Yin W, Wang X, Liu H, Wang Y, Nocker S, Tu M, Fang J, Guo J, Li Z, Wang X (2022) Overexpression of VqWRKY31 enhances powdery mildew resistance in grapevine by promoting salicylic acid signaling and specific metabolite synthesis. Horticulture Research 9:uhab064.
Zhou Q, Du Y, Cheng S, Li R, Zhang J, Wang Y (2015) Resveratrol derivatives in four tissues of six wild Chinese grapevine species. New Zealand Journal of Crop and Horticultural Science 43:204-213
图文来源:植物生物技术Pbj