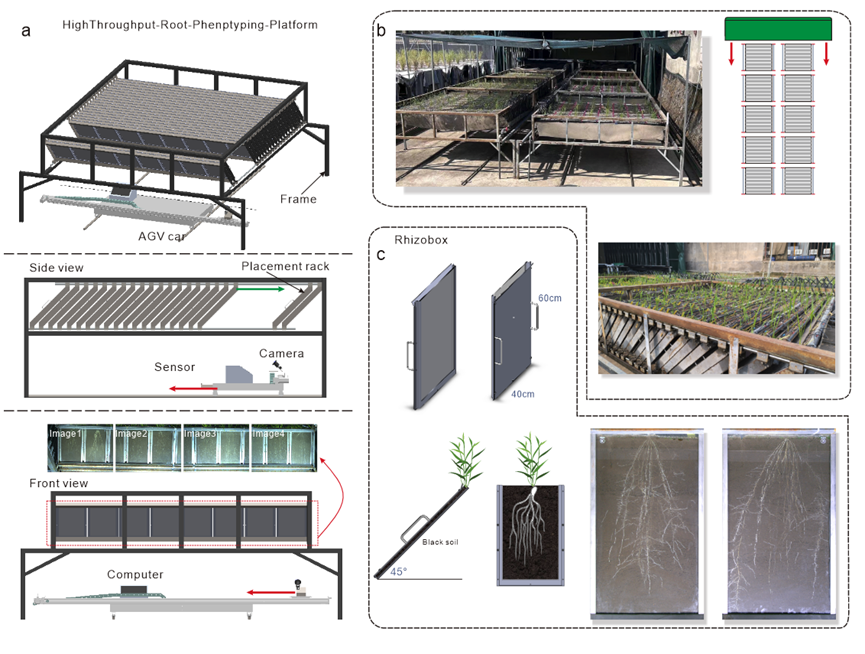
该研究为了解决这一问题,自主研发了一套高通量根系表型平台(图1),包括根盒系统、自动数据采集、智能灌溉等核心模块,实现大规模、精准、高效的根系生长监测。该平台由根盒、支架、自动导引车(AGV)、电动伸缩遮雨装置等组成,可同时测定1680株幼苗的根系生长动态。根盒采用矩形结构(高60 cm、宽30 cm、厚1.5 cm),前侧、两侧及底部由钢板封闭,背面嵌入透明玻璃,并倾斜45°放置,以利用根系向地性促使根部贴附玻璃生长,实现高质量成像。自动化成像系统搭载Basler-acA5472工业相机,光轴垂直于玻璃面,结合LED光源均匀照明,相机沿轨道移动,在检测到限位传感器后自动捕获图像,每张图像分辨率5472 × 3648像素,单次扫描可拍摄两组根盒。该平台还配备自动滴灌系统确保精准控水,实现不同环境下的根系生长监测和干旱胁迫实验。
图1 高通量根系表型平台


原文链接:
https://onlinelibrary.wiley.com/doi/10.1111/pbi.70040
参考文献:
Santos-Medellín, C., Liechty, Z., Edwards, J., Nguyen, B., Huang, B., Weimer, B.C. and Sundaresan, V. (2021) Prolonged drought imparts lasting compositional changes to the rice root microbiome. Nature Plants 7, 1065-1077.
Trachsel, S., Kaeppler, S.M., Brown, K.M. and Lynch, J.P. (2011) Shovelomics: high throughput phenotyping of maize (Zea mays L.) root architecture in the field. Plant Soil 341, 75-87.
Atkinson, J.A., Pound, M.P., Bennett, M.J. and Wells, D.M. (2019) Uncovering the hidden half of plants using new advances in root phenotyping. Current Opinion in Biotechnology 55, 1-8.
Haling, R.E., Tighe, M.K., Flavel, R.J. and Young, I.M. (2013) Application of X-ray computed tomography to quantify fresh root decomposition in situ. Plant Soil 372, 619-627.
van Dusschoten, D., Metzner, R., Kochs, J., Postma, J.A., Pflugfelder, D., Bühler, J., Schurr, U. and Jahnke, S. (2016) Quantitative 3D Analysis of Plant Roots Growing in Soil Using Magnetic Resonance Imaging Plant Physiol 170, 1176-1188.
Metzner, R., Eggert, A., van Dusschoten, D., Pflugfelder, D., Gerth, S., Schurr, U., Uhlmann, N. and Jahnke, S. (2015) Direct comparison of MRI and X-ray CT technologies for 3D imaging of root systems in soil: potential and challenges for root trait quantification. Plant Methods 11, 17.
Seethepalli, A., Dhakal, K., Griffiths, M., Guo, H., Freschet, G.T. and York, L.M. (2021) RhizoVision Explorer: open-source software for root image analysis and measurement standardization. AoB PLANTS 13, plab056.
Matsuda, S., Takano, S., Sato, M., Furukawa, K., Nagasawa, H., Yoshikawa, S., Kasuga, J., Tokuji, Y., Yazaki, K., Nakazono, M., Takamure, I. and Kato, K. (2016) Rice Stomatal Closure Requires Guard Cell Plasma Membrane ATP-Binding Cassette Transporter RCN1/OsABCG5. Mol Plant 9, 417-427.
Zheng, C., Zhou, J., Zhang, F., Yin, J., Zhou, G., Li, Y., Chen, F. and Xie, X. (2020) OsABAR1, a novel GRAM domain-containing protein, confers drought and salt tolerance via an ABA-dependent pathway in rice. Plant Physiol Biochem 152, 138-146.
图文来源:植物生物技术Pbj