近日,Plant Biotechnology Journal杂志在线发表了由南开大学玄元虎课题组和东北林业大学蓝兴国课题组合作的研究论文“Phytochrome B-mediated light signaling enhances rice resistance to saline-alkaline and sheath blight by regulating multiple downstream transcription factors”。该研究工作通过对不同光照条件下水稻耐盐碱及甲基铵(MeA)处理的表型及机制的分析,揭示了PhyB分别与多种不同的下游转录因子的相互作用,最后通过不同的信号通路来调节NH4+的吸收,在促进水稻耐盐碱能力的同时还具有较好的抗水稻纹枯病的能力。研究结果丰富了水稻耐盐碱的信号调控网络,为改良水稻耐盐碱能力及抗纹枯病提供了重要的理论基础。
为了研究光对水稻耐盐碱性的影响,研究者通过在含有100 mM NaCl或80 mM NaHCO3的培养液中进行的幼苗生长实验,比较了水稻根部在全光照和全黑暗条件下的盐害率。研究者观察到在不同光照条件下的盐害率有显著差异(图1a,b),这一现象也表明光信号确实会影响水稻的SAT。作为植物相应光信号的重要受体,因而研究者探究了光敏色素是否在调节水稻的SAT中发挥作用。结果发现仅有phyB突变体的盐害率显著低于野生型Dongjin(DJ)水稻,而phyA和phyC突变体没有显著差异(图1c-e)。有研究表明,NH4+是光调节根系生长的关键因子(Hirano et al. 2008)。进一步探讨这一点,研究者在不同光照条件下用甲基铵(MeA)处理水稻。结果表明不同光照条件下MeA的抑制效果仍存在差异(图1f,g)。为了进一步验证PhyB在调节水稻SAT中的作用,研究者评估了DJ、phyB、AMT1 RNAi和phyB/AMT1 RNAi的盐害率。结果表明,phyB/AMT1 RNAi和AMT1 RNAi的盐害率相似,且显著高于phyB和DJ(图1h-j)。这些结果表明,光敏色素PhyB是光信号介导的水稻SAT的关键调节因子。
图1. PhyB是光信号介导的水稻SAT的关键调节因子
研究团队先前的研究发现,PhyB通过抑制转录因子IDD10和BZR1,进而抑制AMT1;2的表达,来抑制NH4+的吸收(Jung et al. 2023)。研究中发现phyB/idd10积累的NH4+比idd10更多。为进一步解释这一现象,分别用植物甾醇生物合成抑制剂propiconazole(PCZ)的处理了phyB/idd10和idd10突变体,并检测了NH4+的水平。结果显示,phyB/idd10突变体在PCZ处理后仍积累了更多的NH4+(图2a),这提示PhyB可能通过IDD10-BZR1以外的途径调节NH4+的吸收。随后,对PhyB的互作蛋白进行筛选,找到了受NH4+诱导的蛋白激酶CIPK31,后续的实验也确认CIPK31与PhyB在细胞质和细胞核中均有相互作用(图2c-e)。而且这一互作关系并不会影响CIPK31的稳定性或PhyB自身的定位(图2f,g)。此外,研究者还发现cipk31突变体中NH4+积累量降低,根部的AMT1表达水平也下降,CIPK31 OX植株则相反(图2h-k),表明CIPK31参与调控AMT1的表达水平,同时由于CIPK31 OX上调了AMT1的表达水平,积累更多了NH4+,也相应地表现出增强的SAT(图2i-q)。
图2. PhyB与CIPK31互作,影响AMT1表达。
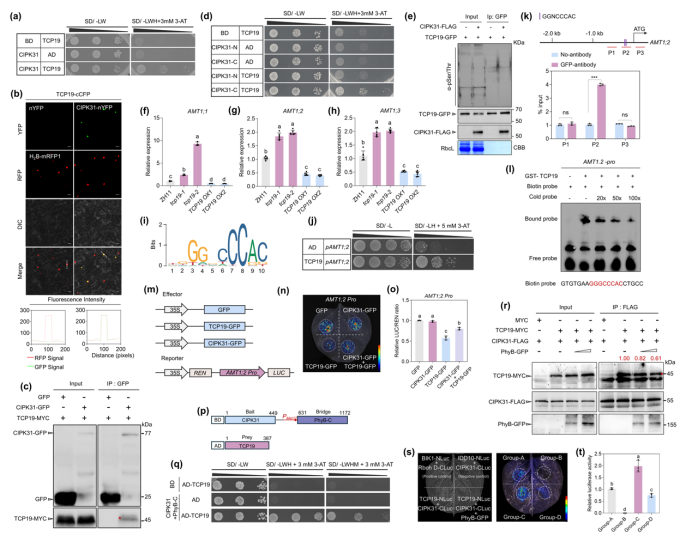
由于蛋白激酶CIPK31无法直接靶向AMT1调控其表达,研究者进而筛选了CIPK31的互作蛋白,找到了水稻中氮利用效率(NUE)关键调节因子的TCP19(Liu et al. 2021),证实了CIPK31通过的C端的非磷酸化结构域与TCP19相互作用(图3a-e)。由于TCP19是NUE的关键转录因子,研究者也分析了其对AMT1基因表达的情况。RT-qPCR和转录组数据发现,tcp19突变体中AMT1的表达上调,而TCP19 OXs中的AMT1下调表达(图3f-h)。同时为了确定TCP19是否直接调控AMT1基因表达,研究者对AMT1启动子序列进行分析,仅在AMT1;2启动子上找到了潜在的TCP19结合基序。随后酵母单杂交(Y1H)实验确认,TCP19直接结合AMT1;2启动子,但不与AMT1;1或AMT1;3启动子结合(图3i,j)。研究者同样利用了染色质免疫沉淀(ChIP)和电泳迁移率实验(EMSA)进一步证实了TCP19能够在体内和体外特异性结合AMT1;2启动子(图3k,i)。结合双荧光素酶报告实验(DLR)的结果表明,TCP19通过直接结合AMT1;2启动子抑制其表达(图3m-o)。DLR实验结果还发现,CIPK31本身并不激活或抑制AMT1;2。然而,CIPK31与TCP19共表达时,减弱了TCP19对AMT1;2的抑制作用(图3m-o),这表明CIPK31可能通过抑制TCP19的抑制作用来影响AMT1;2启动子的活性。
研究者还发现拟南芥PIF同源物,PhyB相互作用蛋白PIL15,也与TCP19存在相互作用(图4a-c)。RT-qPCR结果表明,PIL15 OXs植株中的AMT1;2表达水平显著高于野生型ZH11,而pil15突变体中低于ZH11。研究者也进一步检测了PIL15是否能结合AMT1;2启动子,随后的Y1H、ChIP和EMSA实验表明,PIL15可以在体内和体外直接结合AMT1;2启动子上的PBE-box基序(图4d-g)。DLR结果显示,当PIL15可以激活AMT1;2的表达。有趣的是,当与TCP19共同表达时,PIL15显著抑制了TCP19介导的AMT1;2抑制作用,仍表现出对AMT1;2的激活作用(图4h-j)。由于PIL15直接激活AMT1;2的表达,研究者同样检测了PIL15植物对盐碱的耐受性。PIL15 OX2植物表现出较高的SAT(图4k),而pil15-2突变体对盐碱处理更加敏感,PIL15 OX2/AMT1 RNAi植物的盐害率高于PIL15 OX2(图4k-m)。在对MeA的敏感性的检测中,PIL15 OX2根系对MeA更为敏感,相较于PIL15 OX2/AMT1 RNAi和pil15-2植物,根长缩短更多(图4n,o)。这些生化和遗传学研究结果表明,AMT1;2是PIL15的直接靶基因,PIL15通过激活AMT1;2表达,积极调节水稻盐碱耐性和NH4+的吸收。
图4. PIL15-TCP19模块平衡AMT1;2调控。
鉴于NH4+的吸收能够增强水稻对ShB的抗性(Wu et al. 2022),研究者检测了PhyB及其相互作用蛋白在ShB抗性中的作用。与NH4+吸收趋势一致,phyB突变体表现出较强的ShB抗性,而PhyB OX则更易感(图5a-d)。CIPK31和TCP19植物也观察到了类似的结果。TCP19通过抑制AMT1;2,减少了NH4+的吸收,负调控ShB抗性(图5e, f),而CIPK31通过减弱TCP19介导的AMT1;2抑制作用,正调控ShB抗性(图5g-j)。有趣的是,与PIL15 OXs植物增强的SAT(图4k-m)不同,pil15突变体对ShB的抗性较强,而PIL15 OX植物的抗性低于野生型ZH11,这与以往研究结果一致(Yuan et al. 2023)(图5k, l)。这些结果表明,与PhyB相互作用转录因子在水稻对耐盐碱性和纹枯病抗性的反应中有着不同的机制。
图5. PhyB信号网络通过调控NH4+吸收协调SAT与ShB抗性
https://onlinelibrary.wiley.com/doi/full/10.1111/pbi.14599
Fankhauser, C., and M. Chen. 2008. ‘Transposing phytochrome into the nucleus’, Trends Plant Sci, 13: 596-601.
Han, R., L. Ma, Y. Lv, L. Qi, J. Peng, H. Li, Y. Zhou, P. Song, J. Duan, J. Li, Z. Li, W. Terzaghi, Y. Guo, and J. Li. 2023. ‘SALT OVERLY SENSITIVE2 stabilizes phytochrome-interacting factors PIF4 and PIF5 to promote Arabidopsis shade avoidance’, Plant Cell, 35: 2972-96.
Hirano, T., Y. Satoh, A. Ohki, R. Takada, T. Arai, and H. Michiyama. 2008. ‘Inhibition of ammonium assimilation restores elongation of seminal rice roots repressed by high levels of exogenous ammonium’, Physiol Plant, 134: 183-90.
Huang, J., Z. Y. Qiu, J. He, H. S. Xu, K. Wang, H. Y. Du, D. Gao, W. N. Zhao, Q. G. Sun, Y. S. Wang, P. Z. Wen, Q. Li, X. O. Dong, X. Z. Xie, L. Jiang, H. Y. Wang, Y. Q. Liu, and J. M. Wan. 2023. ‘Phytochrome B mediates dim-light-reduced insect resistance by promoting the ethylene pathway in rice’, Plant Physiol, 191: 1272-87.
Jung, J. H., Z. Li, H. Chen, S. Yang, D. Li, R. A. Priatama, V. Kumar, and Y. H. Xuan. 2023. ‘Mutation of phytochrome B promotes resistance to sheath blight and saline-alkaline stress via increasing ammonium uptake in rice’, Plant J, 113: 277-90.
Li, Jing-Yi, Xing-Guang Deng, Li-Juan Chen, Fa-Qiong Fu, Xiao-Jun Pu, De-Hui Xi, and Hong-Hui Lin. 2015. ‘Involvement of PHYB in resistance to Cucumber mosaic virus in Nicotiana tabacum’, Plant Growth Regulation, 77: 33-42.
Liu, Y., H. Wang, Z. Jiang, W. Wang, R. Xu, Q. Wang, Z. Zhang, A. Li, Y. Liang, S. Ou, X. Liu, S. Cao, H. Tong, Y. Wang, F. Zhou, H. Liao, B. Hu, and C. Chu. 2021. ‘Genomic basis of geographical adaptation to soil nitrogen in rice’, Nature, 590: 600-05.
Ma, L., R. Han, Y. Yang, X. Liu, H. Li, X. Zhao, J. Li, H. Fu, Y. Huo, L. Sun, Y. Yan, H. Zhang, Z. Li, F. Tian, J. Li, and Y. Guo. 2023. ‘Phytochromes enhance SOS2-mediated PIF1 and PIF3 phosphorylation and degradation to promote Arabidopsis salt tolerance’, Plant Cell, 35: 2997-3020.
Quail, Peter H., Margaret T. Boylan, Brian M. Parks, Timothy W. Short, Yong Xu, and Doris Wagner. 1995. ‘Phytochromes: Photosensory Perception and Signal Transduction’, Science, 268: 675-80.
Sambade, Adrian, Amitesh Pratap, Henrik Buschmann, Richard J. Morris, and Clive Lloyd. 2012. ‘The Influence of Light on Microtubule Dynamics and Alignment in the Arabidopsis Hypocotyl’, The Plant Cell, 24: 192-201.
Wu, X. X., P. Yuan, H. Chen, V. Kumar, S. M. Kang, B. Jia, and Y. H. Xuan. 2022. ‘Ammonium transporter 1 increases rice resistance to sheath blight by promoting nitrogen assimilation and ethylene signalling’, Plant Biotechnol J, 20: 1085-97.
Yuan, P., S. Yang, L. Feng, J. Chu, H. Dong, J. Sun, H. Chen, Z. Li, N. Yamamoto, A. Zheng, S. Li, H. C. Yoon, J. Chen, D. Ma, and Y. H. Xuan. 2023. ‘Red-light receptor phytochrome B inhibits BZR1-NAC028-CAD8B signaling to negatively regulate rice resistance to sheath blight’, Plant Cell Environ, 46: 1249-63.
Zhao, Y., H. Shi, Y. Pan, M. Lyu, Z. Yang, X. Kou, X. W. Deng, and S. Zhong. 2023. ‘Sensory circuitry controls cytosolic calcium-mediated phytochrome B phototransduction’, Cell, 186: 1230-43.e14.
图文来源:植物生物技术Pbj






