本文内容速览:
研究一个基因的功能,我们知道可以对其过表达、敲除/干扰以及回补的方式进行验证,通过观察转基因材料的表型判断该基因是否具有某种功能,这些手段是研究基因功能的常规方法,那么除了这些常见的转基因材料之外,我们是否也可以将不同的基因组合进行转基因来实现更多的功能解读呢?答案是有的,下面是小远在阅读文献的过程中收集起来的一些比较有代表性的案例,分享给大家,希望给大家的科研带来一丝的灵感与启发。
确定组合基因之间的上下游关系
提到基因之间的上下游关系,往往离不开遗传互作这个概念,遗传互作是指在遗传学中两个或多个基因/蛋白之间发生的相互作用,这种作用影响了它们各自的表型。当两个基因/蛋白互作时,它们联合作用的效果与各自单独作用的效果不同。这种互作可以是表型上的协同作用或拮抗作用,即两个基因/蛋白的效果联合起来可能表现为增强、减弱或产生新的表型。通过遗传互作验证一般可以确定基因/蛋白间的上下游关系。
如何进行遗传互作验证?一般是通过构建需要确定遗传互作关系的两个基因/蛋白的转基因遗传材料,例如双过表达材料或双突变体材料等,通过对转基因遗传材料与野生型材料表型的观察来判断两个基因/蛋白的上下游关系,甚至可以更进一步地判断调控关系。这种在遗传学上证明两个基因/蛋白间上下游关系的方法,小远在“辨清敌我,统一战线——确定基因上下游关系”“辨清敌我,统一战线——确定基因上下游关系(二)”两篇公众号推文有详细介绍。
构建不同基因之间的转基因组合材料除了可以判断基因的上下游关系,也可以根据表型判断组合基因之间是否存在功能依赖/功能冗余,这里的功能依赖严格来说也属于判断基因上下游的范畴,但小远找到了一个较好的案例,所以介绍给大家。
确定组合基因之间的功能依赖
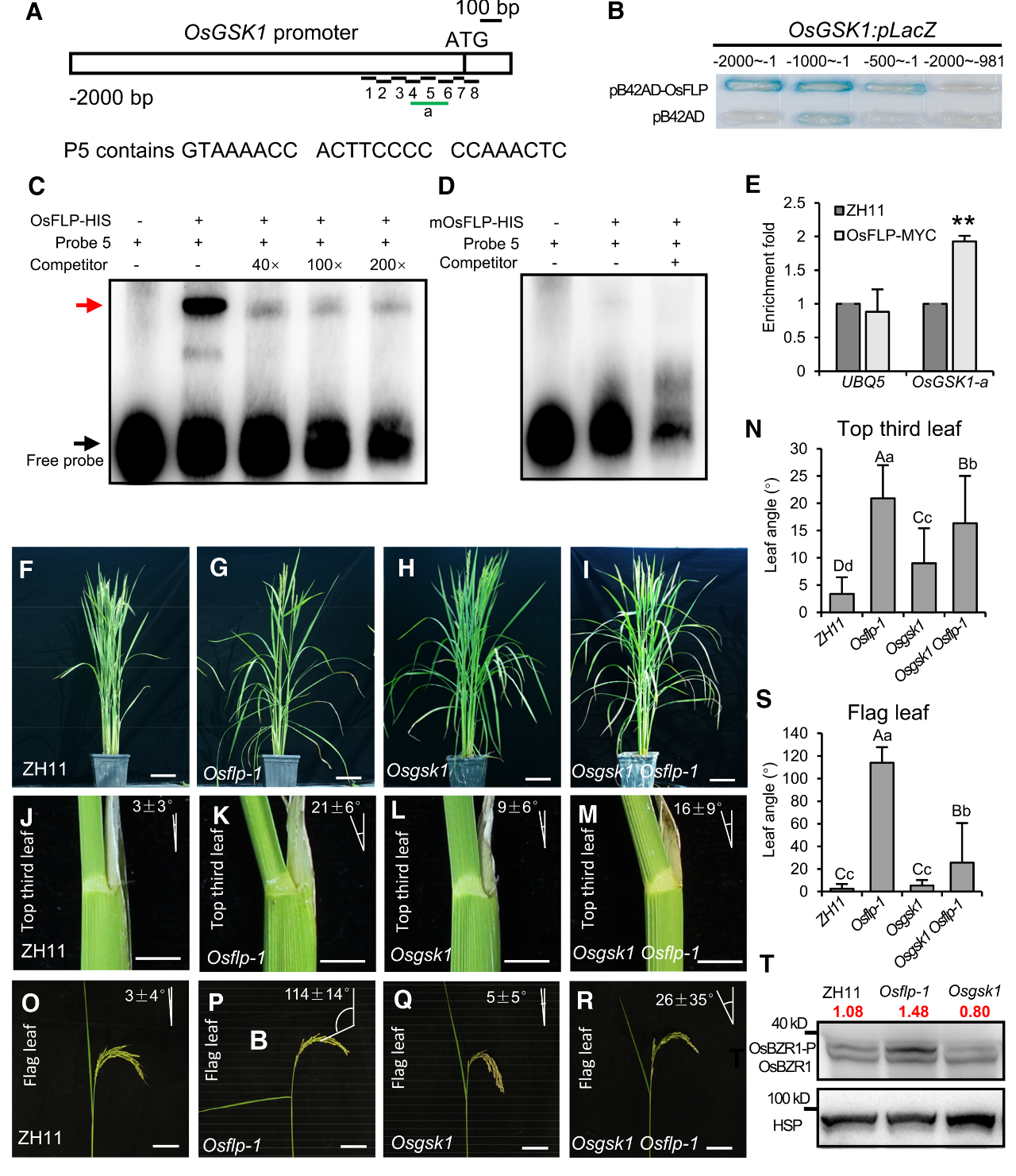
2024年9月,中科院植物所乐捷团队在The Plant Cell杂志上发表了一篇题为“The rice R2R3 MYB transcription factor FOUR LIPS connects brassinosteroid signaling to lignin deposition and leaf angle”的研究论文,该文章鉴定到一个非典型的R2R3-MYB转录因子FOUR LIPS(OsFLP),其在BR信号转导过程中与OsGSK1和OsBZR1协同调节水稻叶枕机械组织中的木质素沉积来维持水稻最适叶夹角。
OsBZR1是BR信号转导的关键转录因子,并且在水稻OsGSKs下游的BR应答中起保守作用。
另外为了帮助大家理解,小远根据文章内容将OsGSK1、OsBZR1以及OsFLP之间的关系进行了展示(图1)。
为了从遗传学上证实OsGSK1受OsFLP的反馈调控,作者通过CRISPR/Cas9基因编辑获得Osgsk1和Osgsk1 Osflp-1突变体。表型分析显示,与ZH11相比,Osgsk1和Osgsk1 Osflp-1植株的植株结构较松散,这种松散的结构与Osflp-1突变体的植株结构相似(图2F-I)。定量分析表明,Osgsk1的第三叶夹角略大于ZH11,但比Osflp-1窄得多。Osgsk1 Osflp-1双突变体的叶夹角介于Osgsk1和Osflp-1之间(图2J-N)。在成熟阶段,与Osflp-1的下垂旗叶表型相反,Osgsk1呈现出与ZH11相似的直立旗叶表型。Osflp-1的下垂旗叶表型在双突变体Osgsk1 Osflp-1中大部分得到恢复,这表明Osflp-1旗叶角度的增加依赖于OsGSK1的抑制信号(图2O-S)。作者用间苯三酚-氯染色法检测了所有突变体叶片顶部第三叶片节的木质素沉积。与Osflp-1类似,Osgsk1和Osgsk1 Osflp-1在叶枕正面和背面的厚壁组织细胞中均显示木质素沉积缺陷。
由于在Osflp-1突变体中没有观察到OsBZR1转录水平的显著变化,因此作者在ZH11、Osflp-1和Osgsk1植物中检测了OsBZR1的磷酸化水平,这对OsBZR1蛋白的稳定性很重要。免疫印迹分析显示Osflp-1中磷酸化的OsBZR1(OsBZR1-P)较多。磷酸化蛋白与非磷酸化蛋白的相对比值由ZH11的1.08增加至Osflp-1的1.48。相比之下,Osgsk1植物中观察到相反的趋势,相对比值下降至0.8,这与OsGSK1在调节OsBZR1磷酸化中的已知作用一致(图2T)。综上所述,OsFLP整合BR信号以维持适当的叶夹角,将OsBZR1介导的BR信号传递给木质素生物合成,并通过OsGSK1-OsBZR1上的反馈回路调节BR信号。
这个案例中表型的观察有点复杂,也有点绕,为了理解清楚其中的关系,大家可以多看几遍结果描述。
两个拟南芥MAPKKs:MKK4和MKK5,在植物生长与发育的多个过程中都位于MPK3/MPK6的上游。YODA(YDA),也被称为MAPKKK4,已被证明是YDA-MKK4/MKK5-MPK3/MPK6 MAPK级联中的MAPKKK,并且在植物生长发育中起信号转导的作用。
据报道,在植物免疫中,MAPKKK3和MAPKKK5是MKK4/MKK5-MPK3/MPK6模块的上游MAPKKKs,形成了由MAPKKK3/MAPKKK5-MKK4/MKK5-MPK3/MPK6组成的完整的MAPK级联。
根据以上信息推测不同的MAPKKKs,如YDA和MAPKKK3/MAPKKK5,可能位于相同的MKK4/MKK5-MPK3/MPK6模块的上游,分别在植物生长/发育和免疫信号传导中形成两个独立的MAPK级联。然而,在响应病原体相关的分子模式(PAMPs)的mapkkk3 mapkkk5双突变体中,仅观察到MPK3/MPK6激活的部分丧失,这表明存在额外的MAPKKK(s),可能与MAPKKK3和MAPKKK5在植物免疫中功能冗余(若不存在功能冗余的基因发挥类似的作用,那么响应PAMPs的mapkkk3 mapkkk5双突变就可以观察到MPK3/MPK6激活的全部丧失)。
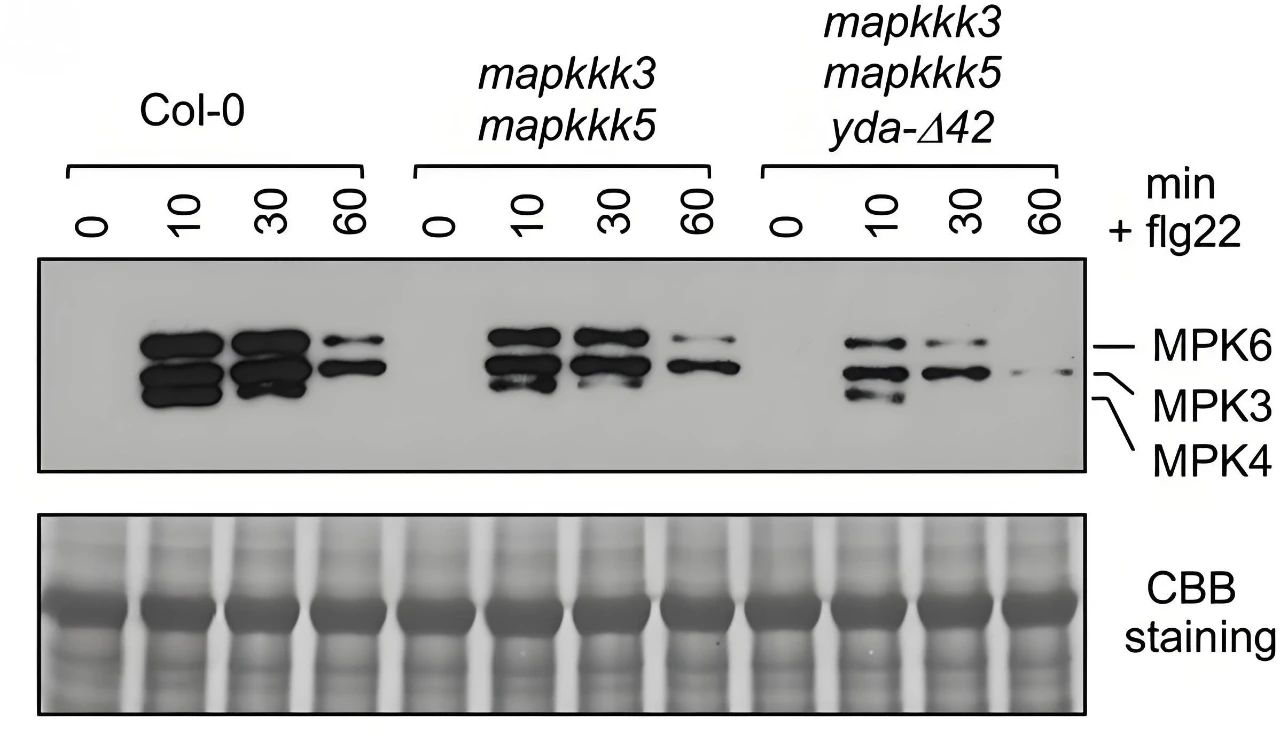
为了测试mapkkk3 mapkkk5 yda-Δ42三突变体中MPK3和MPK6在防御反应中的激活作用,作者用flg22(flg22多肽是细菌鞭毛蛋白N端的一段保守性极高的区域,能够诱导植物天然的免疫反应)对Col-0、mapkkk3 mapkkk5双突变体、mapkkk3 mapkkk5 yda-Δ42三突变体幼苗分别处理不同的时间,并收集样品测定MPK3和MPK6的磷酸化。如图5A所示,在双mapkkk3 mapkkk5突变背景下,YDA功能的部分缺失进一步降低了MPK3/MPK6在flg22作用下的磷酸化,这表明YDA与MAPKKK3和MAPKKK5存在功能冗余。
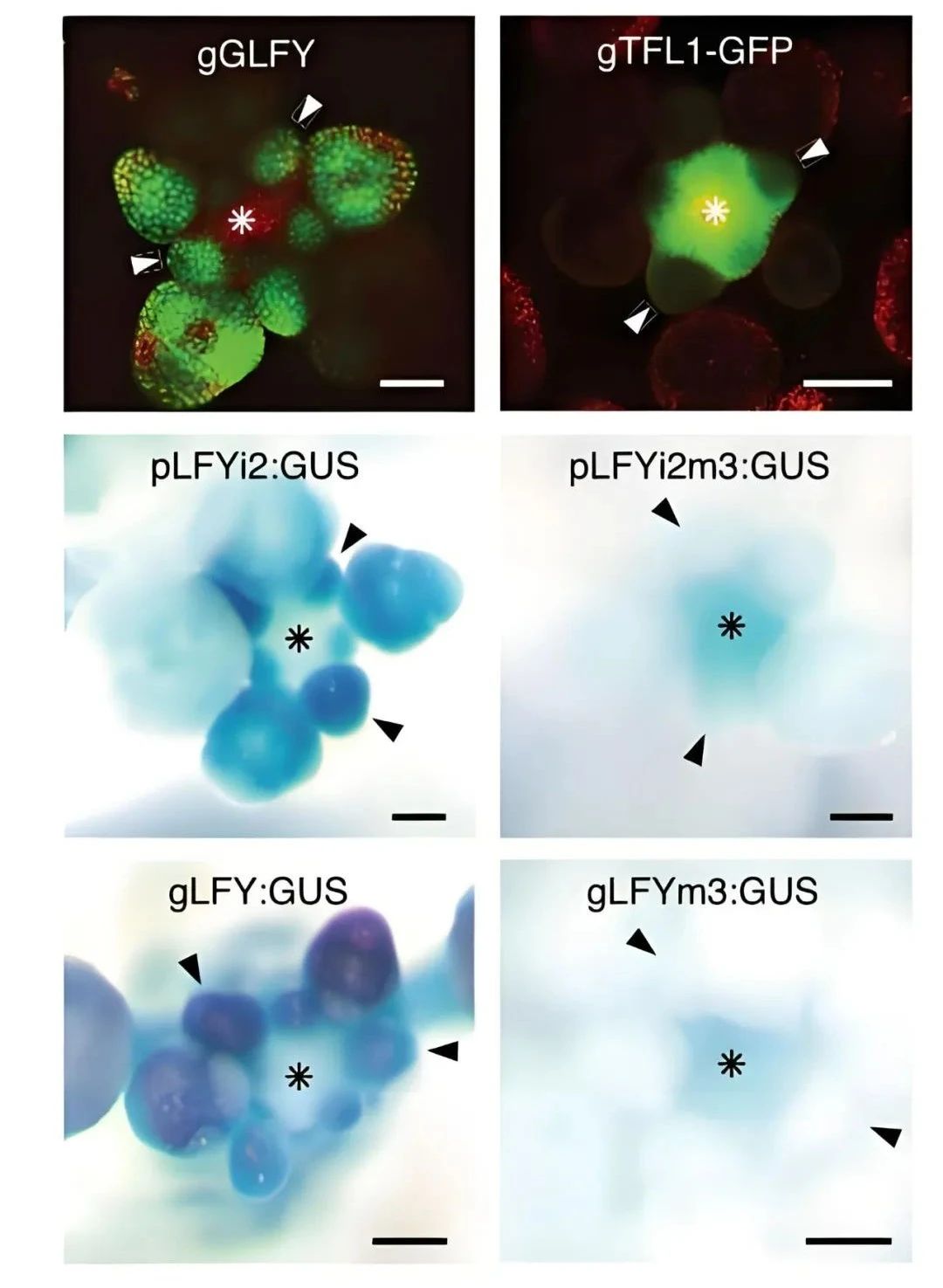
图4 上图:LFY和TFL1蛋白在具有花原基的花序顶端表达;中间和底部:野生型或bZIP结合位点突变(m3)的启动子驱动GUS报告基因(pLFYi2:GUS)或它们的基因组与GUS报告基因融合表达(gLFY-GUS)的中β-葡萄糖苷酸酶的积累(Zhu et al., 2020)。植物在长日照条件下生长。在相同条件下进行染色。箭头:花原基;星号:花序顶端。
上面介绍了利用组织特异性启动子或诱导启动子构建转基因材料的相关方法,但有可能利用这些启动子无法按照预期启动目的基因的表达,那么是什么原因导致目的基因无法表达呢?下面即将讲到的文献案例给出了一种可能的答案,由于其研究思路也值得我们学习借鉴,所以也一起介绍给大家!
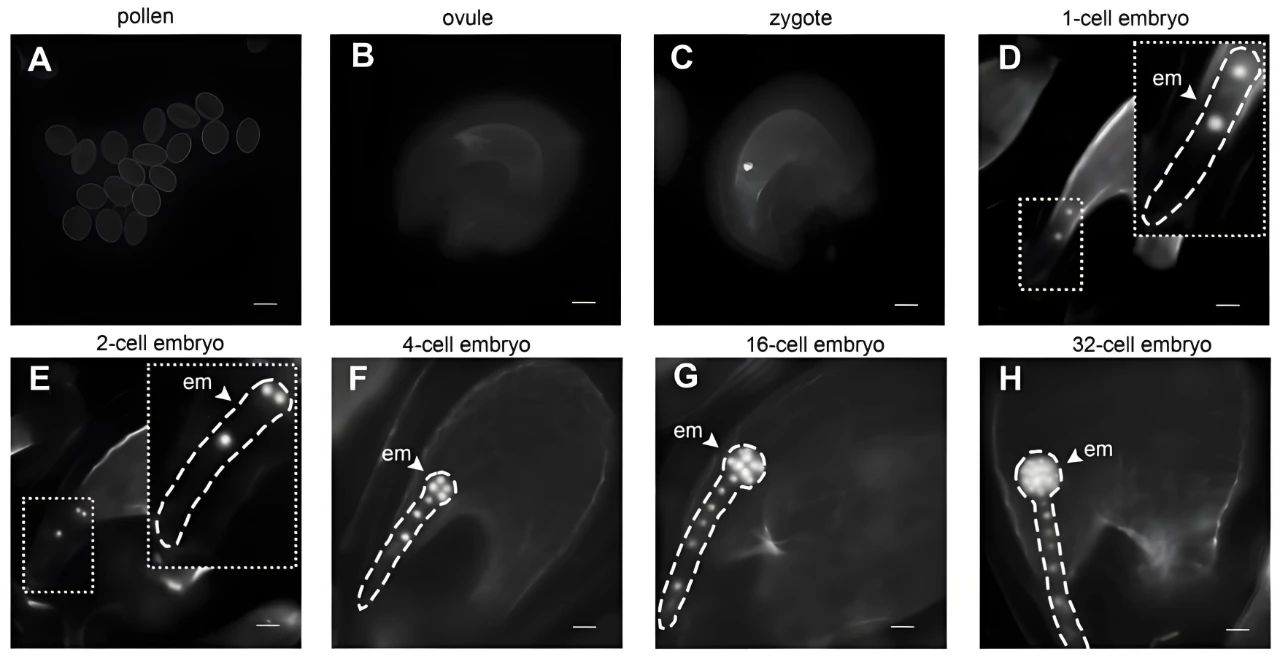
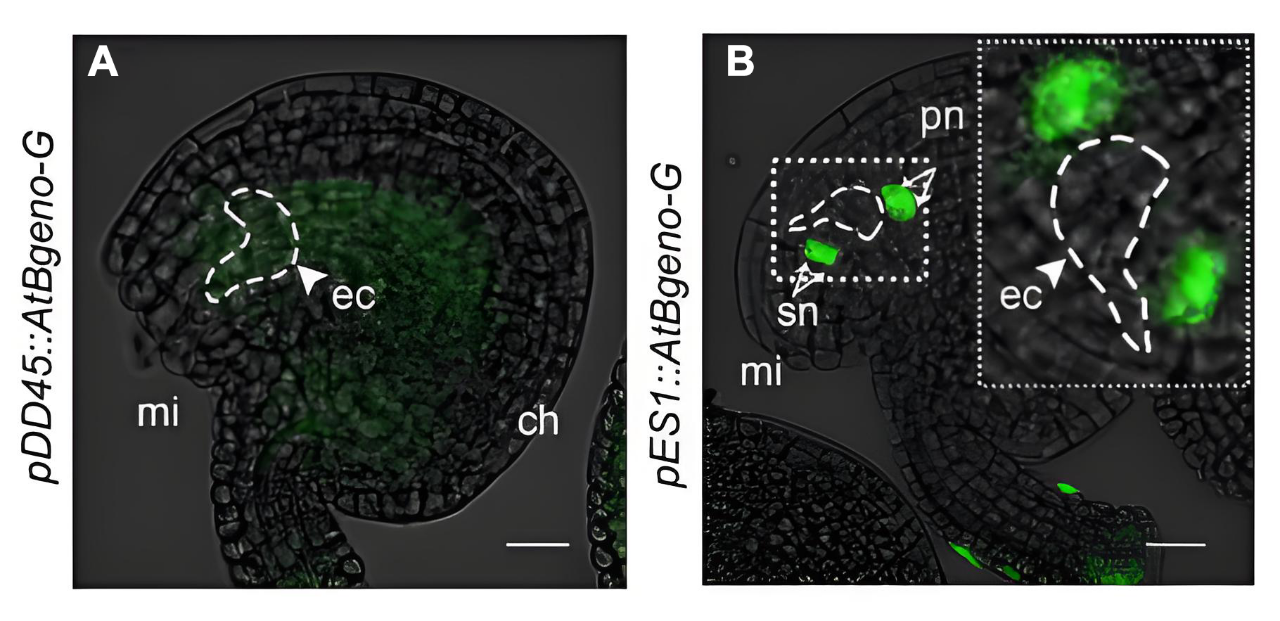
AtBBM基因(BABY BOOM)编码AP2/ERF转录因子,调控拟南芥早期胚胎发育,具有将营养生长向生殖生长转变的潜能。PsASGR–BBML(Ps是非洲狼尾草的缩写)与AtBBM具有高度同源性,并且PsASGR–BBML在玉米、水稻和小米等单子叶植物的卵细胞中异位表达可诱导孤雌生殖并产生单倍体后代。然而拟南芥中AtBBM不能在卵细胞直接表达,双子叶植物中BBM诱导孤雌生殖的机制尚未有明确的解析。为了解析该机制,作者进行了一系列的探究。
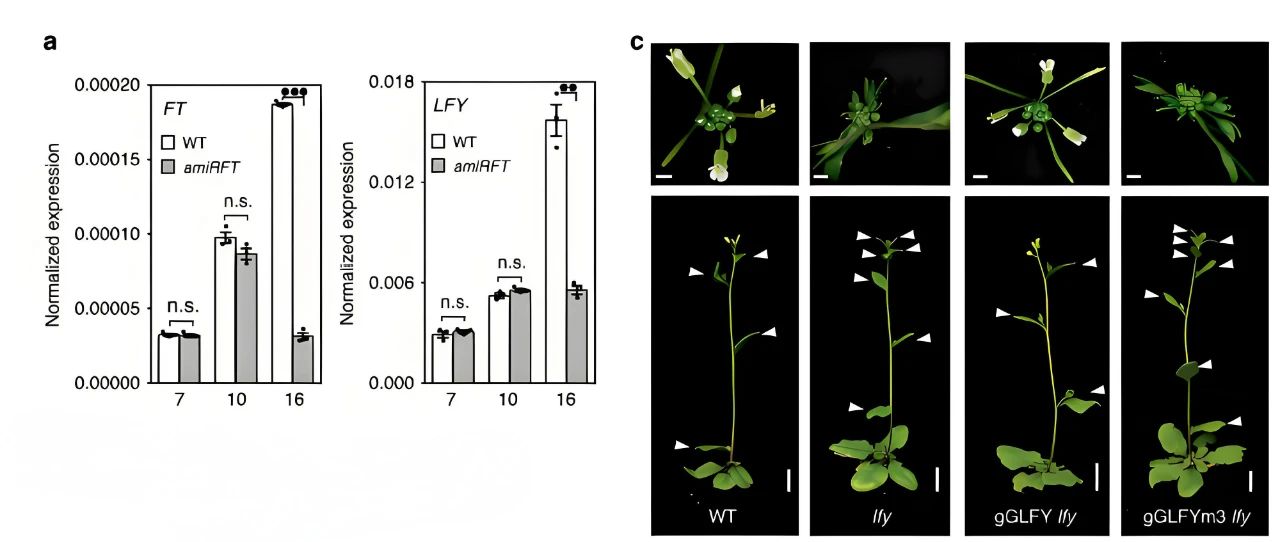
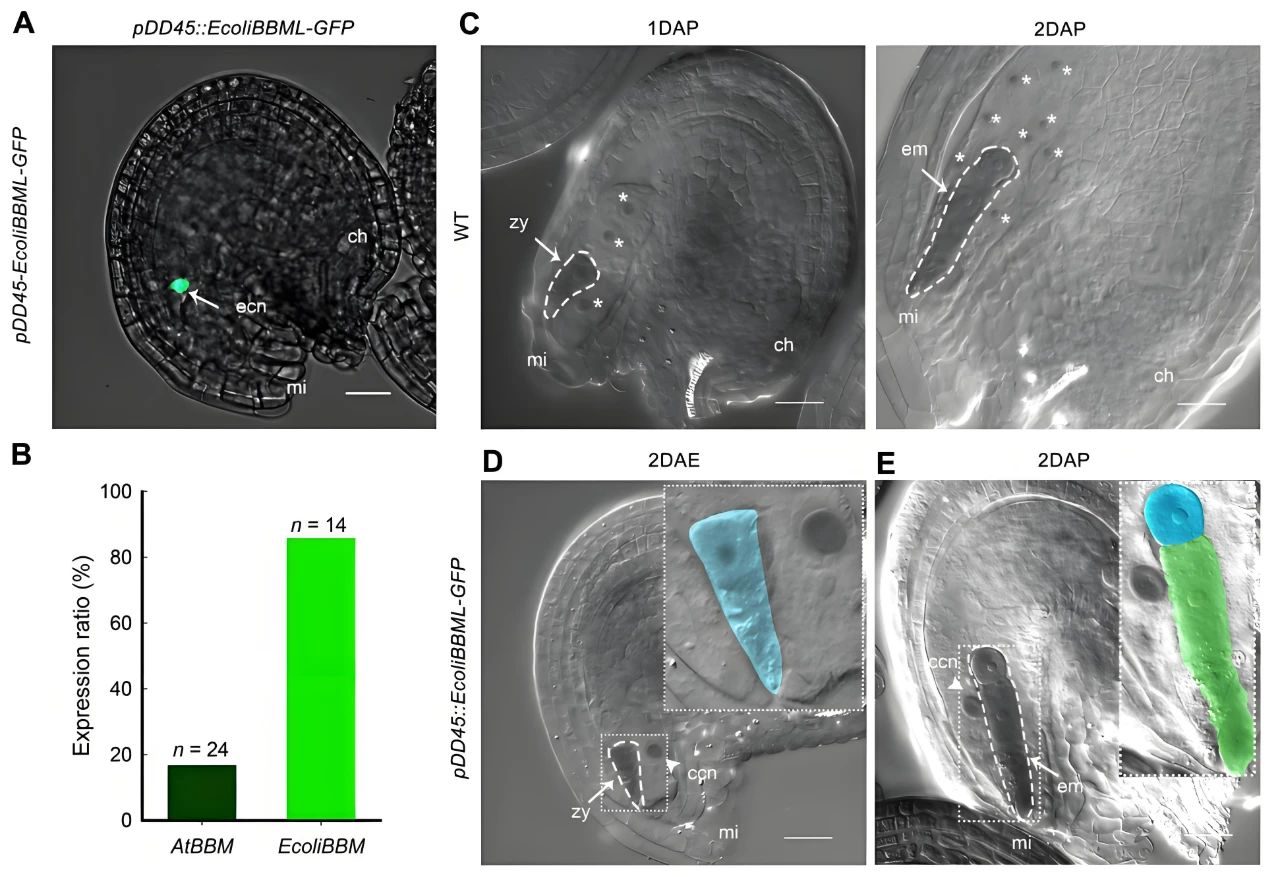
在不改变氨基酸序列的情况下,根据大肠杆菌密码子偏好,将AtBBM的编码序列改变为类似于远亲大肠杆菌BBM基因(EcoliBBM)的编码序列,并将EcoliBBM基因在拟南芥中异位过表达,在转基因植株中,85.71%(12/14)的卵细胞可检测到荧光,这一发现表明EcoliBBM在卵细胞中的异位表达可以降低BBM表达的潜在抑制作用,从而使AtBBM在卵细胞中的异位表达成为可能。另外通过表型分析以及育性分析,在没有受精的情况下胚胎发育的开始证实了BBM基因诱导孤雌生殖的能力。
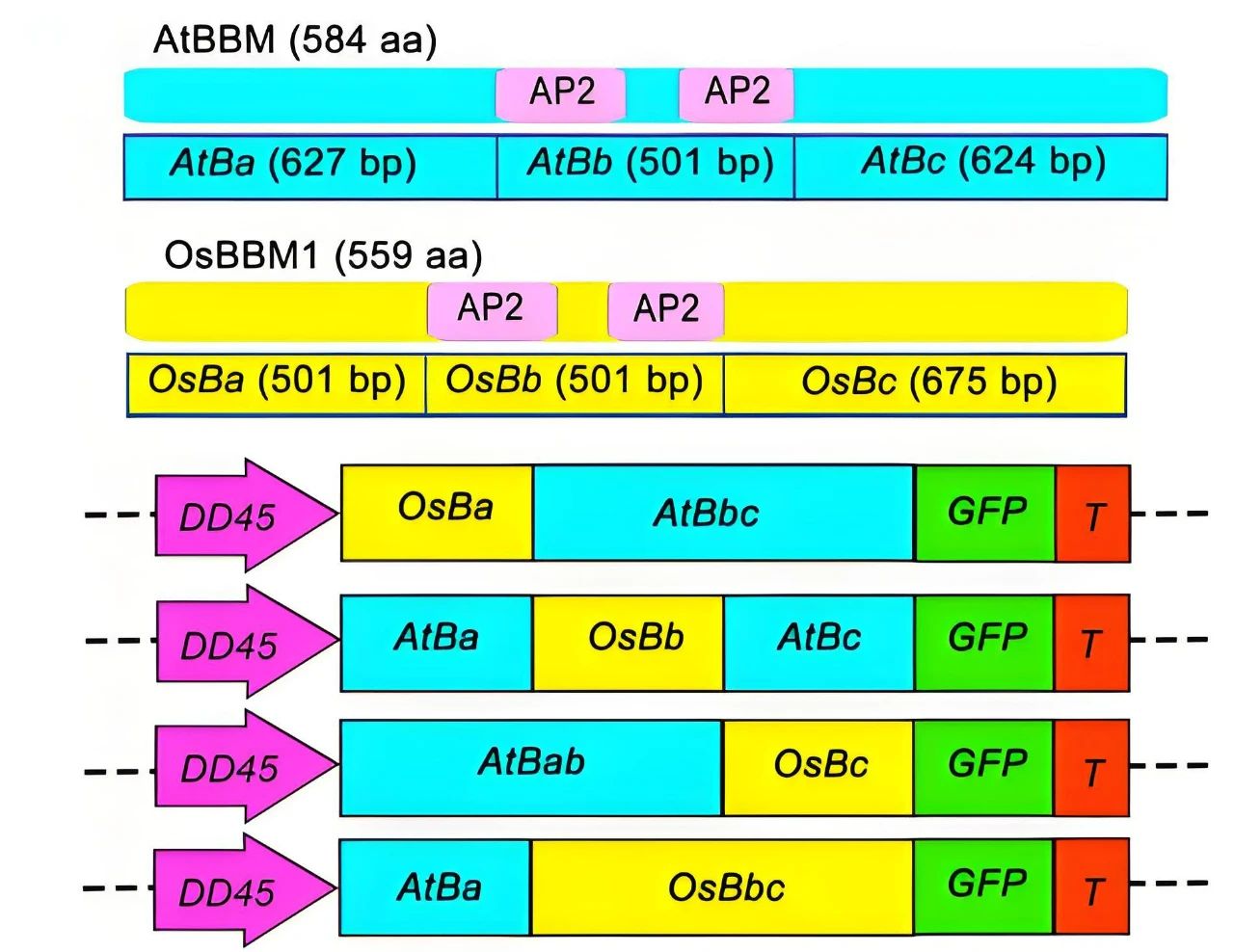
为了确定BBM基因的潜在抑制因子,作者以BBM基因的c段为诱饵进行酵母单杂交(Y1H)筛选。结果发现转录因子AtRKD与AtBBM的c段特异性结合,而a段和b段没有这种相互作用。作者通过双荧光素酶实验结合转录组数据证明AtRKD5抑制AtBBM的表达。
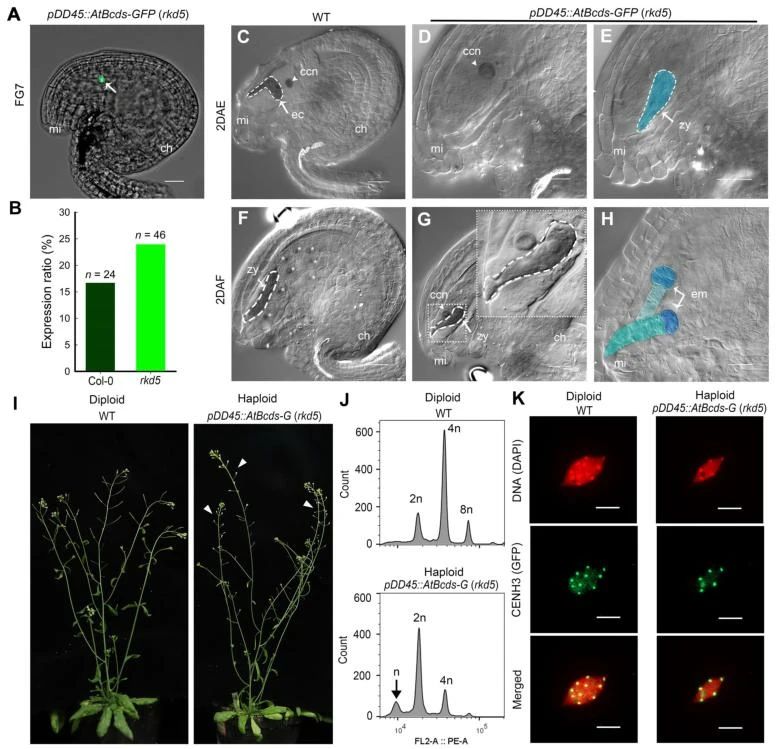
为了在体内验证AtRKD5对AtBBM的抑制作用,作者在rkd5-3突变体的卵细胞中异位过表达AtBBMcds。26.09%(12/46)转基因植株的卵细胞可检测到荧光,高于野生型AtBBM直接异位表达的效率(图10A、B),表明AtRKD5突变可增强AtBBM在卵细胞中的异位表达,并且诱导孤雌生殖得到单倍体后代,实现双子叶植物中利用内源BBM基因诱导孤雌生殖。
图10 在atrkd5突变体中,AtBBM的异位表达启动孤雌生殖并诱导单倍体后代(Liu et al., 2024)。(A)在rkd5-3突变体中,AtBBMcds使用pDD45启动子在卵细胞中异位表达,表达水平高于Col-0植物;(B)异位表达的效率被量化为卵细胞衍生的荧光植株与转基因植株总数的比值(n);(C)在野生型植物中,去雄后2天,胚珠中卵细胞和中心细胞的形态保持不变;(D、E)在atrkd5突变体中,去雄后2天,AtBBM在卵细胞中的异位表达触发了卵细胞的独立发育,导致合子样结构的形成;(F)在野生型植物中,授粉后2天,中心细胞和卵细胞分别发育为胚乳和胚;(G、H)在atrkd5突变体中,授粉后2天,AtBBM在卵细胞中的异位表达导致孤雌胚胎(G)的形成和双胚胎(H)在胚珠中的发生;(I)atrkd5突变体卵细胞中AtBBMcds异位表达后代的育性分析。单倍体植物表现出明显的不育表型;(J)atrkd5突变体卵细胞中AtBBMcds异位表达后代的流式细胞术分析;(K)atrkd5突变体卵细胞中异位表达AtBBMcds子代的免疫荧光研究。染色体用抗着丝粒组蛋白CENH3的抗体标记。
References:
Liu H, Zhang J, Wang J, et al. The rice R2R3 MYB transcription factor FOUR LIPS connects brassinosteroid signaling to lignin deposition and leaf angle[J]. The Plant Cell, 2024, 36(11): 4768-4785.
Liu Q, Han D, Cheng D, et al. AtRKD5 inhibits the parthenogenic potential mediated by AtBBM[J]. Journal of Integrative Plant Biology, 2024.
Liu Y, Leary E, Saffaf O, et al. Overlapping functions of YDA and MAPKKK3/MAPKKK5 upstream of MPK3/MPK6 in plant immunity and growth/development[J]. Journal of Integrative Plant Biology, 2022, 64(8): 1531-1542.
Schwab R, Ossowski S, Riester M, et al. Highly specific gene silencing by artificial microRNAs in Arabidopsis[J]. The Plant Cell, 2006, 18(5): 1121-1133.
Zhu Y, Klasfeld S, Jeong C W, et al. TERMINAL FLOWER 1-FD complex target genes and competition with FLOWERING LOCUS T. Nat Commun 11: 5118[EB/OL].(2020)
图文来源:伯远生物公众号